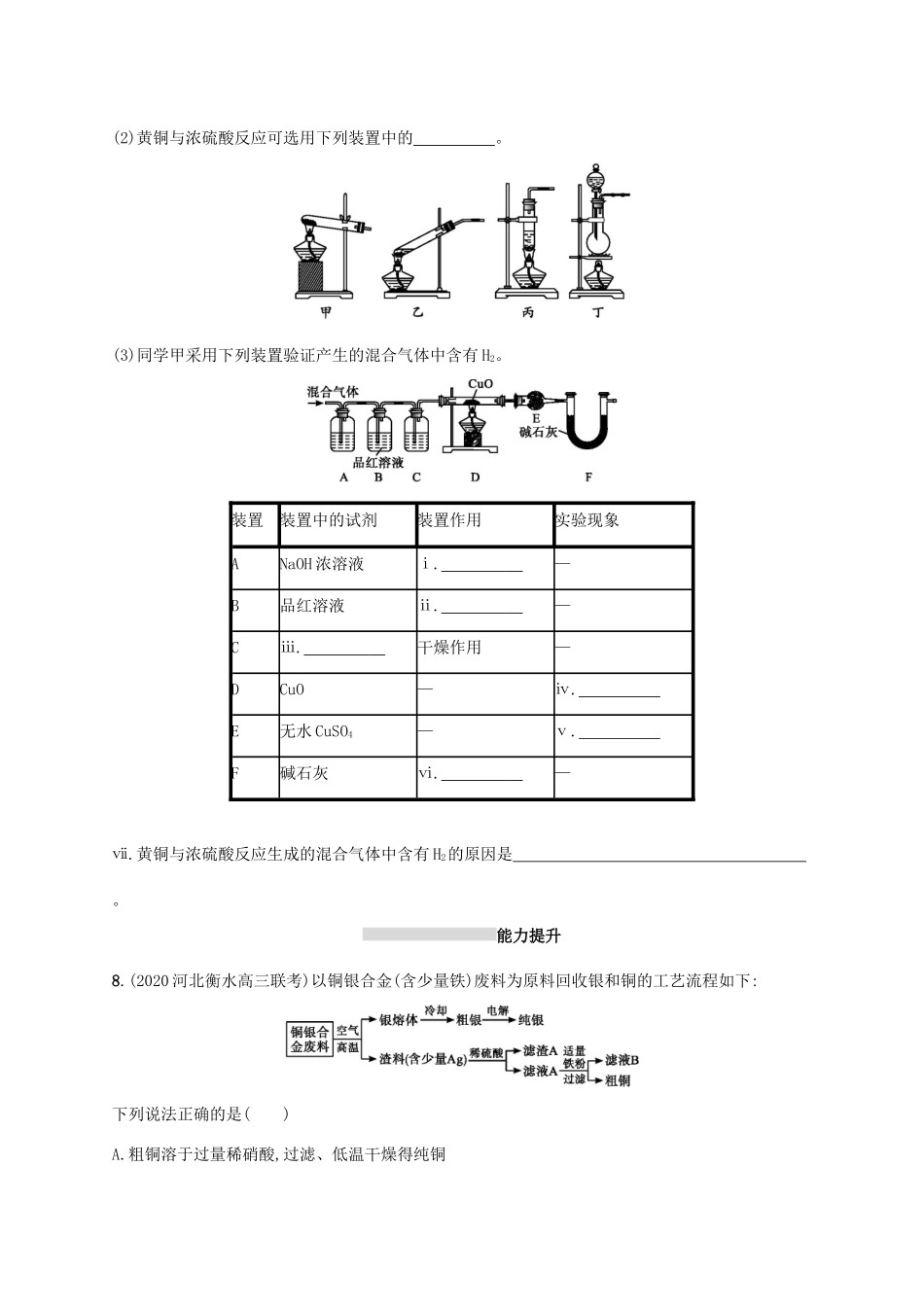
课时规范练9铜及其重要化合物用途广泛的金属材料基础巩固1.金属材料在日常生活以及生产中有着广泛的应用。下列关于金属的一些说法不正确的是()A.合金的性质与其组成金属的性质不完全相同B.火烧孔雀石[Cu2(OH)2CO3]制得铜也属于还原法C.金属冶炼的本质是金属阳离子得到电子变成金属原子D.工业上金属Mg、Cu都是用热还原法制得的2.明代宋应星著的《天工开物》中有关于“火法”冶炼锌的工艺记载:“炉甘石十斤,装载入一泥罐内,……然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,……,冷淀,毁罐取出,……,即倭铅也。”下列说法不正确的是(注:炉甘石的主要成分为碳酸锌)()A.该冶炼锌的反应属于置换反应B.煤炭中起作用的主要成分是CC.冶炼Zn的反应方程式为ZnCO3+2CZn+3CO↑D.倭铅是指金属锌和铅的混合物3.(2019黑龙江哈尔滨月考)下列说法中正确的是()A.纯铁易被腐蚀,可以在纯铁中混入碳元素制成“生铁”,以提高其抗腐蚀能力B.我们使用合金是因为它比纯金属具有更优良的化学性质C.我国首艘航母“辽宁舰”上用于舰载机降落的拦阻索是特种钢缆,属于金属材料D.Na、Al、Cu可以分别用电解冶炼法、热还原法和热分解法得到4.(2020广西南宁模拟)某化学小组为测定一定质量的某铜铝混合物中铜的质量分数,设计了如下实验方案:方案Ⅰ:铜铝混合物测定生成气体的体积方案Ⅱ:铜铝混合物测定剩余固体的质量下列有关判断中不正确的是()A.溶液A和B均可以是盐酸或NaOH溶液B.若溶液B选用浓硝酸,则测得铜的质量分数偏小C.溶液A和B均可选用稀硝酸D.实验室中方案Ⅱ更便于实施5.(2019湖南师大附中月考)下列说法中正确的是()A.Cu→CuO→Cu(OH)2每步转化均能通过一步反应实现B.铝合金是一种混合物,它比纯铝的熔点高C.金属铜放置在潮湿的空气中会被锈蚀,生成绿色的铜锈——碱式碳酸铜D.金属铝、铁、铜都有一定的抗腐蚀性能,其抗腐蚀的原因都是表面形成氧化物薄膜,阻止反应的进一步进行6.(2020江西九江调研)某同学利用下列实验探究金属铝与铜盐溶液的反应:下列说法正确的是()A.由实验1可以得出结论:金属铝的活泼性弱于金属铜B.实验2中生成红色物质的离子方程式为Al+Cu2+Al3++CuC.溶液中阴离子种类不同是导致实验1、2出现不同现象的原因D.由上述实验可推知:用砂纸打磨后的铝片分别与H+浓度均为0.2mol·L-1的盐酸和硫酸反应,后者更剧烈7.铜是一种重要的金属元素,其单质、合金和化合物具有广泛的用途。黄铜色如黄金,成分为铜锌合金。某学校化学学习小组的同学在实验室中对黄铜与浓硫酸的反应进行了下面的探究。(1)写出Cu与浓硫酸反应生成SO2的化学方程式:(2)黄铜与浓硫酸反应可选用下列装置中的。(3)同学甲采用下列装置验证产生的混合气体中含有H2。装置装置中的试剂装置作用实验现象ANaOH浓溶液ⅰ.—B品红溶液ⅱ.—Cⅲ.干燥作用—DCuO—ⅳ.E无水CuSO4—ⅴ.F碱石灰ⅵ.—ⅶ.黄铜与浓硫酸反应生成的混合气体中含有H2的原因是。能力提升8.(2020河北衡水高三联考)以铜银合金(含少量铁)废料为原料回收银和铜的工艺流程如下:下列说法正确的是()A.粗铜溶于过量稀硝酸,过滤、低温干燥得纯铜B.电解时用粗银作阴极,硝酸银溶液为电解质溶液C.用稀硫酸处理渣料时主要发生了氧化还原反应D.从滤液B中可以提取绿矾(FeSO4·7H2O)9.CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法不正确的是()A.将CuSO4溶液蒸发浓缩、冷却结晶可制得胆矾晶体B.相对于途径①、③,途径②更好地体现了绿色化学思想C.CuSO4在1100℃分解所得气体X可能是SO2和SO3的混合气体D.Y具有还原性10.新制氢氧化铜悬浊液中存在如下平衡:Cu(OH)2+2OH-[Cu(OH)4]2-(深蓝色)。某同学进行下列实验:下列说法不正确的是()A.①中出现蓝色沉淀B.③中现象是平衡Cu(OH)2+2OH-[Cu(OH)4]2-正向移动的结果C.④中现象证明葡萄糖具有还原性D.对比②和④可知Cu(OH)2氧化性强于[Cu(OH)4]2-11.某同学设计了如下实验测量mg铜银合金样品中铜的质量分数:下列说法中不正确的是()A.合金的熔点比其成分金属低,通常比成分金属具有更优良的金属特性B.铜银都能与稀硝酸反应,收集到的VL气体全为NOC.操作Ⅰ是过滤,操作Ⅱ是洗涤D.铜的质量分数为143.5V-22.4W100.4m×100%12.(2020湖北武汉二中调...