溶解度曲线考点面面观1
判断或比较溶解度的大小例1(2008年·南昌市)下图为氯化钠、碳酸钠(俗称纯碱)在水中的溶解度曲线
(1)当温度为10℃时,碳酸钠的溶解度为________g
(2)当温度________时,氯化钠的溶解度大于碳酸钠的溶解度
(3)生活在盐湖附近的人们习惯“夏天晒盐,冬天捞碱”
请你解释原因:_________
分析:由溶解度曲线可知,10℃时碳酸钠的溶解度为10g;当温度小于30℃时氯化钠的溶解度大于碳酸钠的溶解度;氯化钠的溶解度受温度的影响不大,可采用蒸发结晶的方法碳酸钠的溶解度受温度的影响较大,可采用冷却热饱和溶液结晶的方法
答案:(1)10(2)小于30℃(3)“夏天晒盐”的原因是氯化钠的溶解度受温度的影响不大,夏天气温高,水易蒸发,氯化钠很容易结晶析出;“冬天捞碱”的原因是碳酸钠的溶解度受温度的影响较大,冬天气温低,碳酸钠的溶解度小,很容易从溶液中析出例2(2008年·台州市)如下图所示,A、B、C表示三种固体物质的溶解度曲线
t2℃时,A、B、C三种物质中溶解度最大的是________
当温度升高时,________的饱和溶液中会有晶体析出
分析:由图像可知t2℃时,A、B、C三种物质的溶解度大小顺序是A>B>C,可知溶解度最大的是A;因物质C的溶解度随温度的升高而减小,所以当温度升高时,物质c的饱和溶液中会有晶体析出
答案:AC2
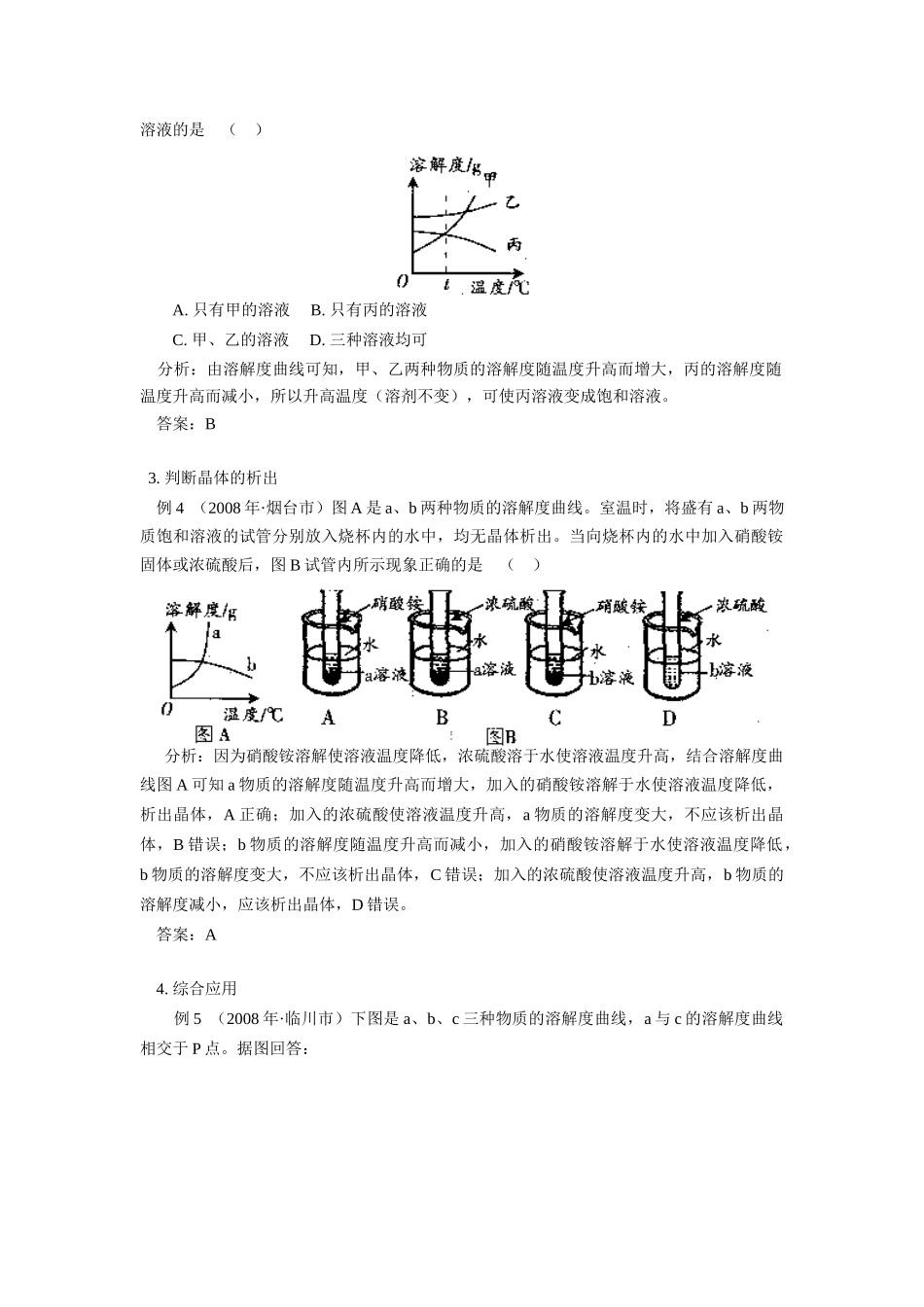
判断两种溶液的转化情况例3(2008年·金华市)如下图所示是甲、乙、丙三种固体物质的溶解度曲线
在t℃时,将甲、乙、丙分别配制成接近饱和的溶液,升高温度(溶剂不变),可使其变成饱和溶液的是()A
只有甲的溶液B
只有丙的溶液C
甲、乙的溶液D
三种溶液均可分析:由溶解度曲线可知,甲、乙两种物质的溶解度随温度升高而增大,丙的溶解度随温度升高而减小,所以升高温度(溶剂不变),可使丙溶液变成饱和溶液