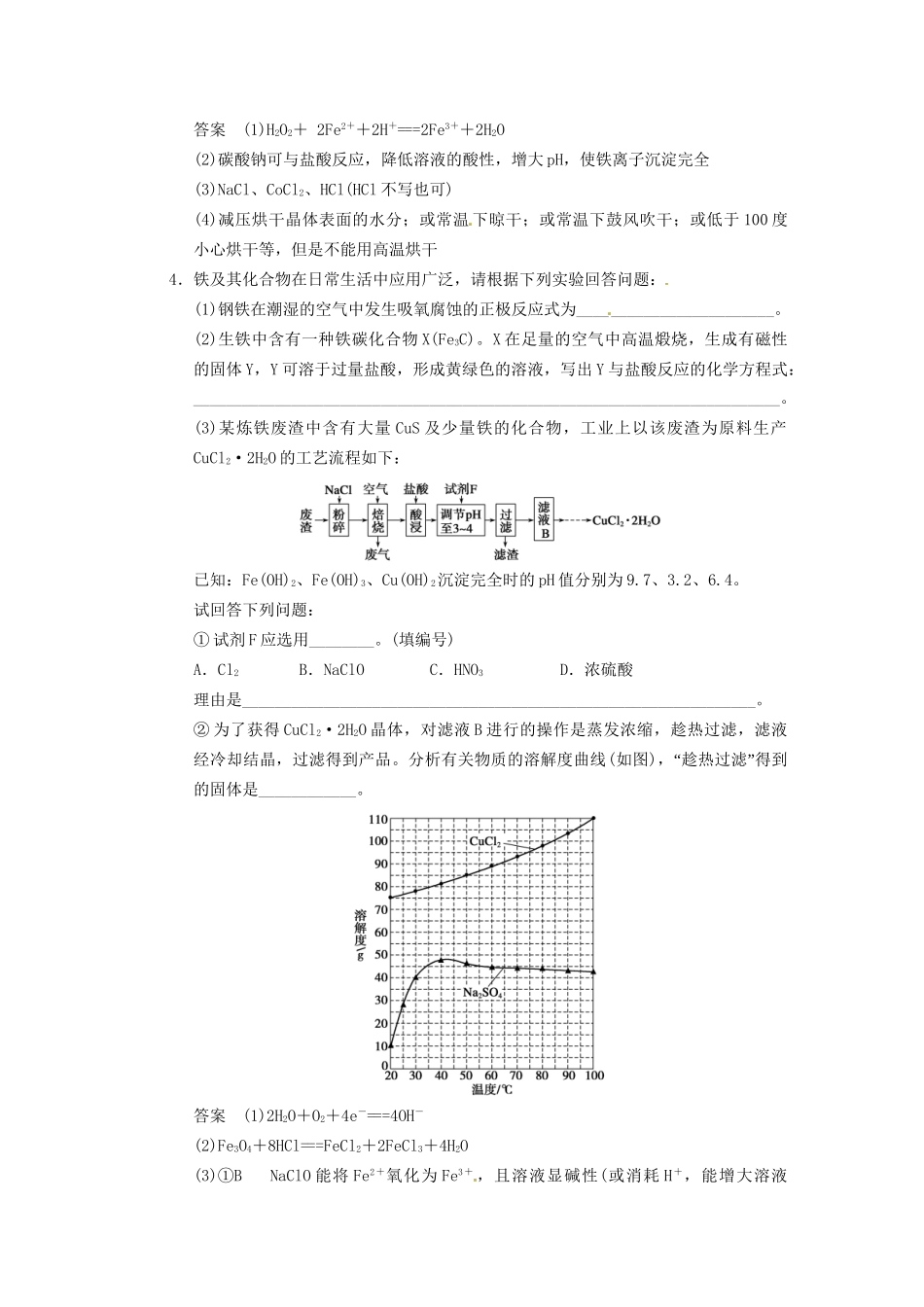
大题冲关滚动练之二——无机化工流程题1.活性氧化锌用作橡胶硫化的活性剂、补强剂。以氧化锌粗品为原料制备活性氧化锌的生产工艺流程如下:一些阳离子以氢氧化物形式完全沉淀时溶液的pH见下表:沉淀物Fe(OH)3Cu(OH)2Zn(OH)2Fe(OH)2pH3.26.78.09.7(1)“”溶解前将氧化锌粗品粉碎成细颗粒,目的是____________________________。(2)“”溶解后得到的酸性溶液中含有Zn2+、SO,另含有Fe2+、Cu2+等杂质。先加入__________(“填Na2CO3”“或H2SO4”)调节溶液的pH至5.4,然后加入适量KMnO4,Fe2+转化为Fe(OH)3,同时KMnO4转化为MnO2。经检测溶液中Fe2+的浓度为0.009mol·L-1,则每升溶液中至少应加入________molKMnO4。(3)杂质Cu2+可利用置换反应除去,应选择的试剂是____________________________。(4)“”沉淀得到ZnCO3·2Zn(OH)2·H2O“”,煅烧在450~500℃“”下进行,煅烧反应的化学方程式为___________________________________________________。答案(1)增大固液接触面积,加快溶解时的反应速率(2)Na2CO30.003(3)锌粉(4)ZnCO3·2Zn(OH)2·H2O=====3ZnO+CO2↑+3H2O↑2.以下是用硫铁矿烧渣(主要成分为Fe2O3、Fe3O4、FeO、SiO2)为原料制备高纯氧化铁的生产流程示意图:回答下列问题:(1)酸浸、过滤后滤液A中的金属阳离子是_________________________________。(2)煅烧FeCO3生成产品Ⅰ的化学反应方程式为_____________________________。(3)已知几种盐的溶解度随温度变化的曲线如下图所示,产品Ⅱ的化学式为____________,为了获得产品Ⅱ,向(NH4)2SO4溶液中加入KCl溶液后,还需要进行的操作是______________、趁热过滤、洗涤、干燥。(4)检验产品Ⅱ晶体中是否含有少量的氯化物杂质需用到的试剂是_______________,进一步提纯产品Ⅱ的方法是________________;(5)步骤Ⅲ中可选用______________(填序号)试剂调节溶液的pH。A.稀硝酸B.双氧水C.氨水D.高锰酸钾溶液答案(1)Fe3+、Fe2+(或铁离子、亚铁离子)(2)4FeCO3+O2===2Fe2O3+4CO2(3)K2SO4蒸发结晶(4)Ba(NO3)2溶液、AgNO3溶液重结晶(5)C3.有关钴和铁化合物的性质见下表分子式溶度积Ksp沉淀完全时的pH氯化钴晶体的性质Co(OH)25.9×10-159.4CoCl2·6H2O呈红色,常温下稳定。110~120℃时脱水变成蓝色无水氯化钴Fe(OH)21.6×10-149.6Fe(OH)31.1×10-363.7用含钴废料(含少量铁)可制备氯化钴:Co+2HCl===CoCl2+H2↑。工艺流程如下:试回答:(1)“”净化除铁中,写出加入H2O2时反应的离子方程式______________________________________________________________________。(2)②步中用Na2CO3调pH≈4的原因是___________________________________。(3)“”滤液中所含主要溶质的化学式是____________。(4)为防止CoCl2·6H2O“”脱水,干燥时可采用的方法或操作是__________。答案(1)H2O2+2Fe2++2H+===2Fe3++2H2O(2)碳酸钠可与盐酸反应,降低溶液的酸性,增大pH,使铁离子沉淀完全(3)NaCl、CoCl2、HCl(HCl不写也可)(4)减压烘干晶体表面的水分;或常温下晾干;或常温下鼓风吹干;或低于100度小心烘干等,但是不能用高温烘干4.铁及其化合物在日常生活中应用广泛,请根据下列实验回答问题:(1)钢铁在潮湿的空气中发生吸氧腐蚀的正极反应式为________________________。(2)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,Y可溶于过量盐酸,形成黄绿色的溶液,写出Y与盐酸反应的化学方程式:________________________________________________________________________。(3)某炼铁废渣中含有大量CuS及少量铁的化合物,工业上以该废渣为原料生产CuCl2·2H2O的工艺流程如下:已知:Fe(OH)2、Fe(OH)3、Cu(OH)2沉淀完全时的pH值分别为9.7、3.2、6.4。试回答下列问题:①试剂F应选用________。(填编号)A.Cl2B.NaClOC.HNO3D.浓硫酸理由是_______________________________________________________________。②为了获得CuCl2·2H2O晶体,对滤液B进行的操作是蒸发浓缩,趁热过滤,滤液经冷却结晶,过滤得到产品。分析有关物质的溶解度曲线(如图)“”,趁热过滤得到的固体是____________。答...