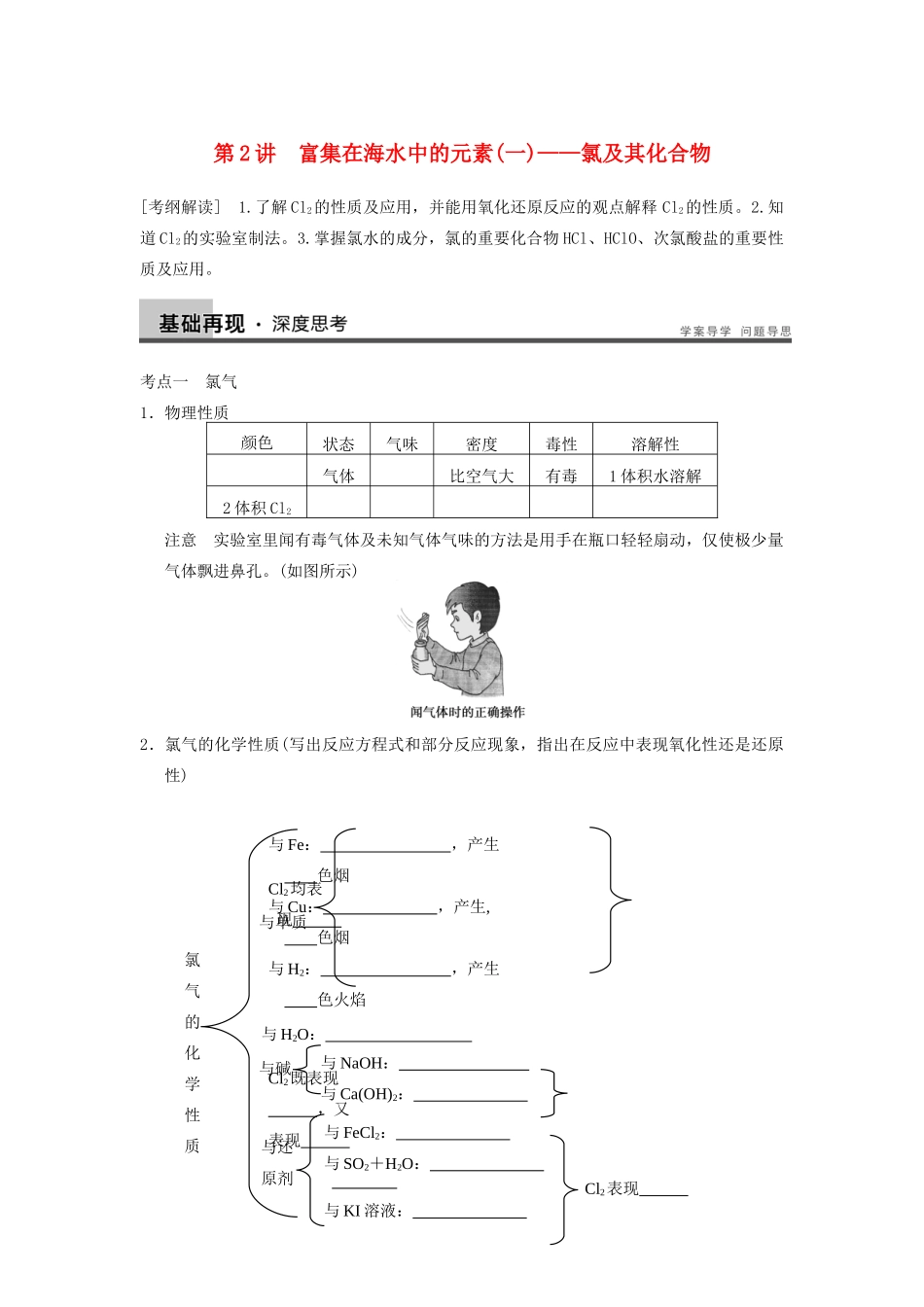
氯气的化学性质与单质与Fe:,产生色烟与Cu:,产生,色烟与H2:,产生色火焰Cl2均表现与H2O:与NaOH:与Ca(OH)2:Cl2既表现,又表现与还原剂与FeCl2:与SO2+H2O:与KI溶液:Cl2表现与碱第2讲富集在海水中的元素(一)——氯及其化合物[考纲解读]1.了解Cl2的性质及应用,并能用氧化还原反应的观点解释Cl2的性质。2.知道Cl2的实验室制法。3.掌握氯水的成分,氯的重要化合物HCl、HClO、次氯酸盐的重要性质及应用。考点一氯气1.物理性质颜色状态气味密度毒性溶解性气体比空气大有毒1体积水溶解2体积Cl2注意实验室里闻有毒气体及未知气体气味的方法是用手在瓶口轻轻扇动,仅使极少量气体飘进鼻孔。(如图所示)2.氯气的化学性质(写出反应方程式和部分反应现象,指出在反应中表现氧化性还是还原性)1.如遇到氯气泄漏应如何自救?2.下列氯化物中,既能由金属和氯气直接反应得到,又能由金属和盐酸反应制得的是()A.FeCl2B.AlCl3C.FeCl3D.CuCl23.把氯气通入下列各物质的溶液中,阴离子和阳离子都能被氧化的是()A.NaOHB.Na2SO3C.FeBr2D.FeSO4考点二几种含氯化合物1.次氯酸(HClO)(1)不稳定性:化学方程式为__________________________________________________。(2)弱酸性:比碳酸酸性____,电离方程式为_____________________________________。(3)强氧化性:具有________性。2.Ca(ClO)2的主要化学性质(1)Ca(ClO)2是________的有效成分,它的稳定性比HClO____。(2)水解显____性,其水解离子方程式:_________________________________________。(3)与酸反应生成________,作为漂白或消毒剂的原理可用化学方程式表示为________________________________________________________________________。4.将Cl2通入石蕊试液中的现象是什么?能用pH试纸测定氯水的pH值吗?5.如何保存氯水、漂白粉?说明原因。6.工业上用Cl2和碱制漂白粉、漂粉精及漂白液。请回答下面的问题:(1)工业上将氯气制成漂粉精的主要目的是______________________________________,制漂粉精的主要反应的化学方程式是___________________________________________。(2)下列物质露置在空气中会变质,在变质过程中既有非氧化还原反应发生,又有氧化还原反应发生的是________。A.生石灰B.漂白粉C.NaOHD.Na2SO3(3)用贮存很久的漂白粉与浓盐酸反应制得的氯气中,可能含有的杂质气体是________(填编号)。①HCl②O2③CO2④H2O(气)氯水成分寻找方法及氯水性质的探究1.氯水成分寻找方法氯水中存在三个平衡关系:(1)Cl2+H2OHCl+HClO(2)HClOH++ClO-(3)H2OH++OH-根据可逆反应的特点,即可得出氯水中存在的各种微粒。2.氯水的多重性质氯水的各种成分决定了它具有多重性质:(1)Cl2——的氧化性与还原性物质反应。如:2FeCl2+Cl2===2FeCl3(除去FeCl3溶液中的FeCl2)SO2+Cl2+2H2O===2HCl+H2SO4(SO2和Cl21∶1混合物通入水中不再具有漂白性)Na2SO3+Cl2+H2O===2HCl+Na2SO4(除去水中的余氯)(2)HCl——酸性和Cl-的性质向NaHCO3溶液中加入氯水,有气泡产生就是利用了盐酸的酸性。加入AgNO3溶液可以检验出氯水中的Cl-,现象是有白色沉淀生成。(3)HClO的氧化性在解释漂白性、杀菌消毒时,使用的是HClO的氧化性。向氯水中滴加紫色石蕊溶液,先变红(H+作用的结果),后褪色(HClO作用的结果)。【例1】某学习小组设计以下四个实验探究氯水的成分,请根据下表回答问题。实验序号实验方法实验现象结论①将氯水滴加到AgNO3溶液中生成白色沉淀②将氯水滴加到含有酚酞的NaOH溶液中③淀粉KI试纸变蓝色氯水中含有Cl2④将足量的氯水滴加到Na2CO3溶液中氯水中含有H+(1)实验①得出的结论______________________________________________________。(2)“”指出实验②和实验④中的实验现象:②________________,④________________________________________________________________________。(3)“”实验③中实验方法的具体操作过程是____________________________________。(4)“”通过实验②的实验现象,同学们得出两个不同的结论。这两个结论可能是a.________________________________________________________...