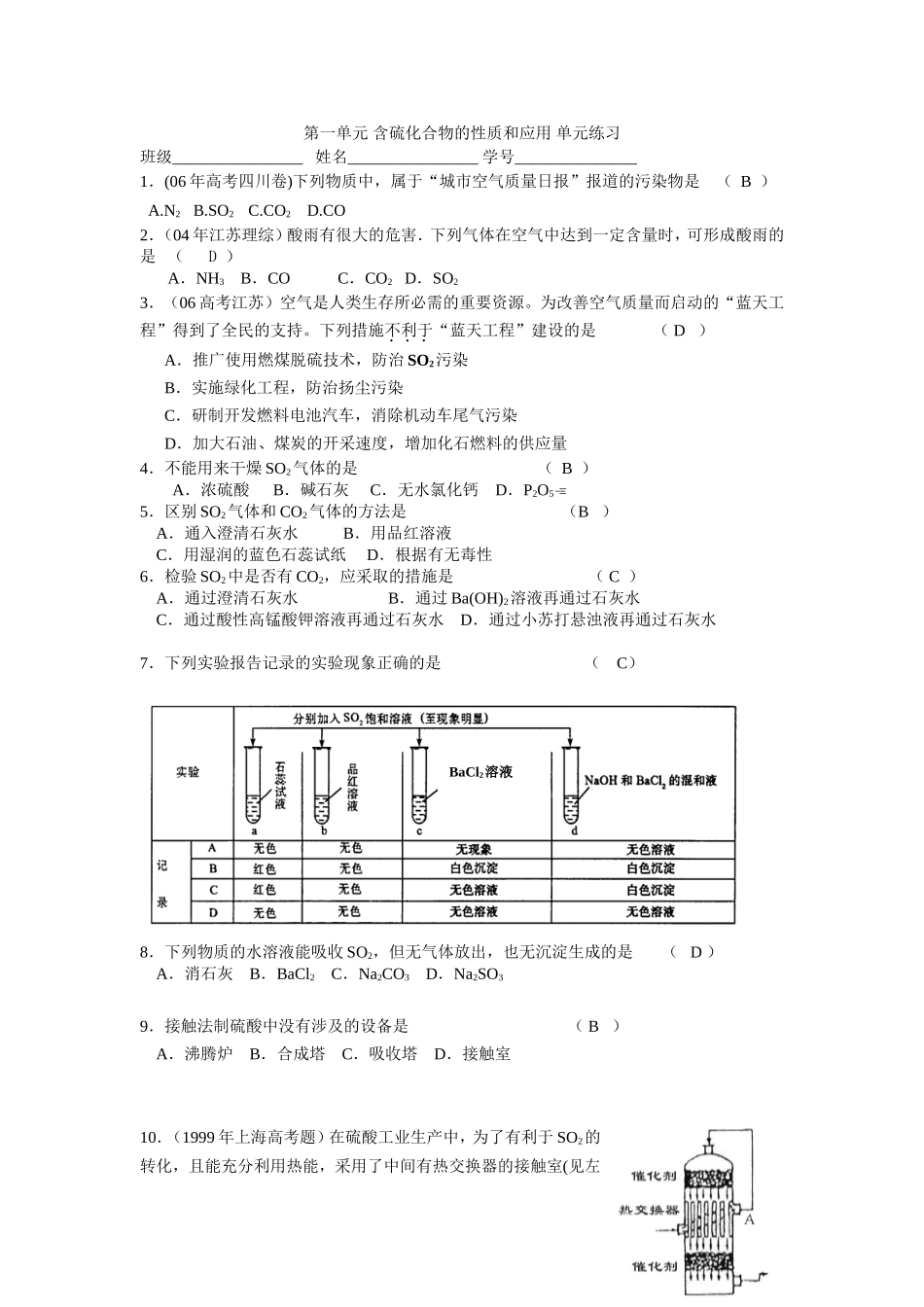
第一单元含硫化合物的性质和应用单元练习班级________________姓名________________学号_______________1.(06年高考四川卷)下列物质中,属于“城市空气质量日报”报道的污染物是(B)A.N2B.SO2C.CO2D.CO2.(04年江苏理综)酸雨有很大的危害.下列气体在空气中达到一定含量时,可形成酸雨的是(D)A.NH3B.COC.CO2D.SO23.(06高考江苏)空气是人类生存所必需的重要资源。为改善空气质量而启动的“蓝天工程”得到了全民的支持。下列措施不利于“蓝天工程”建设的是(D)A.推广使用燃煤脱硫技术,防治SO2污染B.实施绿化工程,防治扬尘污染C.研制开发燃料电池汽车,消除机动车尾气污染D.加大石油、煤炭的开采速度,增加化石燃料的供应量4.不能用来干燥SO2气体的是(B)A.浓硫酸B.碱石灰C.无水氯化钙D.P2O55.区别SO2气体和CO2气体的方法是(B)A.通入澄清石灰水B.用品红溶液C.用湿润的蓝色石蕊试纸D.根据有无毒性6.检验SO2中是否有CO2,应采取的措施是(C)A.通过澄清石灰水B.通过Ba(OH)2溶液再通过石灰水C.通过酸性高锰酸钾溶液再通过石灰水D.通过小苏打悬浊液再通过石灰水7.下列实验报告记录的实验现象正确的是(C)8.下列物质的水溶液能吸收SO2,但无气体放出,也无沉淀生成的是(D)A.消石灰B.BaCl2C.Na2CO3D.Na2SO39.接触法制硫酸中没有涉及的设备是(B)A.沸腾炉B.合成塔C.吸收塔D.接触室10.(1999年上海高考题)在硫酸工业生产中,为了有利于SO2的转化,且能充分利用热能,采用了中间有热交换器的接触室(见左BaCl2溶液图)。按此密闭体系中气体的流向,则在A处流出的气体为(C)A.SO2B.SO3,O2C.SO2,O2D.SO2,SO311.(04年江苏考)下列关于浓硫酸的叙述正确的是(D)A.浓硫酸具有吸水性,因而能使蔗糖炭化B.浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体C.浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体D.浓硫酸在常温下能够使铁、铝等金属钝化*12.在铜和浓H2SO4的反应中,如果电子转移0.4mol,则被还原的硫酸的物质的量是(B)A.0.4molB.0.2molC.2molD.4mol13.含硫48%的硫铁矿煅烧时FeS2损失率为2%,则下列说法不正确的是(A)A.该硫铁矿含FeS2也是48%B.硫损失也是2%C.铁损失也是2%D.该硫铁矿含铁42%二、填空14.SO2是重要的大气污染物,大量SO2的来源是。SO2不仅本身污染大气,而且它在大气中经尘粒催化能与水、氧气作用形成危害更大的酸雨,反应的化学方程式是、。抽取某地酸雨水样进行检验,测得各离子的浓度分别是:c(Na+)=2.3×10-5mol/L,c(Cl-)=2.3×10-5mol/L,c(NH4+)=2.3×10-5mol/L,c(SO42-)=2.3×10-5mol/L,则该酸雨中的c(H+)=。15.为了降低硫的氧化物造成的污染所采用的一种方法是在含硫燃料(如煤)中加入生石灰,这种方法称为“钙基固硫”,采用这种方法在燃烧过程中“固硫”反应的化学方程式为_______________________;__________________________________16.用一定量的废铜制取胆矾有下两种方法:⑴取铜与浓硫酸直接反应,有关化学方程式是:⑵另一种是先将铜在空气中加热使之生成氧化铜,再与稀硫酸反应。有关的化学方程式是:_______________________________________________其中第种方法好,原因是17.为了证实木炭和浓H2SO4的反应产物,可用下列流程进行验证(箭头表示气体的流向)。提示:酸性高锰酸钾溶液或溴水都会氧化SO2气体无水硫酸铜品红试液I品红试液II酸性KMnO4澄清石灰水回答下列问题:(1)根据上述流程中什么现象证明产物是H2O、CO2、SO2:____________________________________________________________________________________________________________________。(2)酸性KMnO4溶液的作用是,能否用溴水代替酸性高锰酸钾溶液?。(填“能”或“不能”)计算18.(04年江苏理综)浓硫酸与铜在加热时反应,生成二氧化硫气体的体积为2.24L(标准状况).试计算:(1)反应后生成硫酸铜的物质的量.(2)若将生成的硫酸铜配制成500mL溶液,则该溶液中溶质的物质的量浓度是多少?第一单元含硫化合物的性质和应用单元练习答案1-5BDDBB6-10CCDBC11-13DBA14.煤和石油的燃烧、金属矿石的冶...