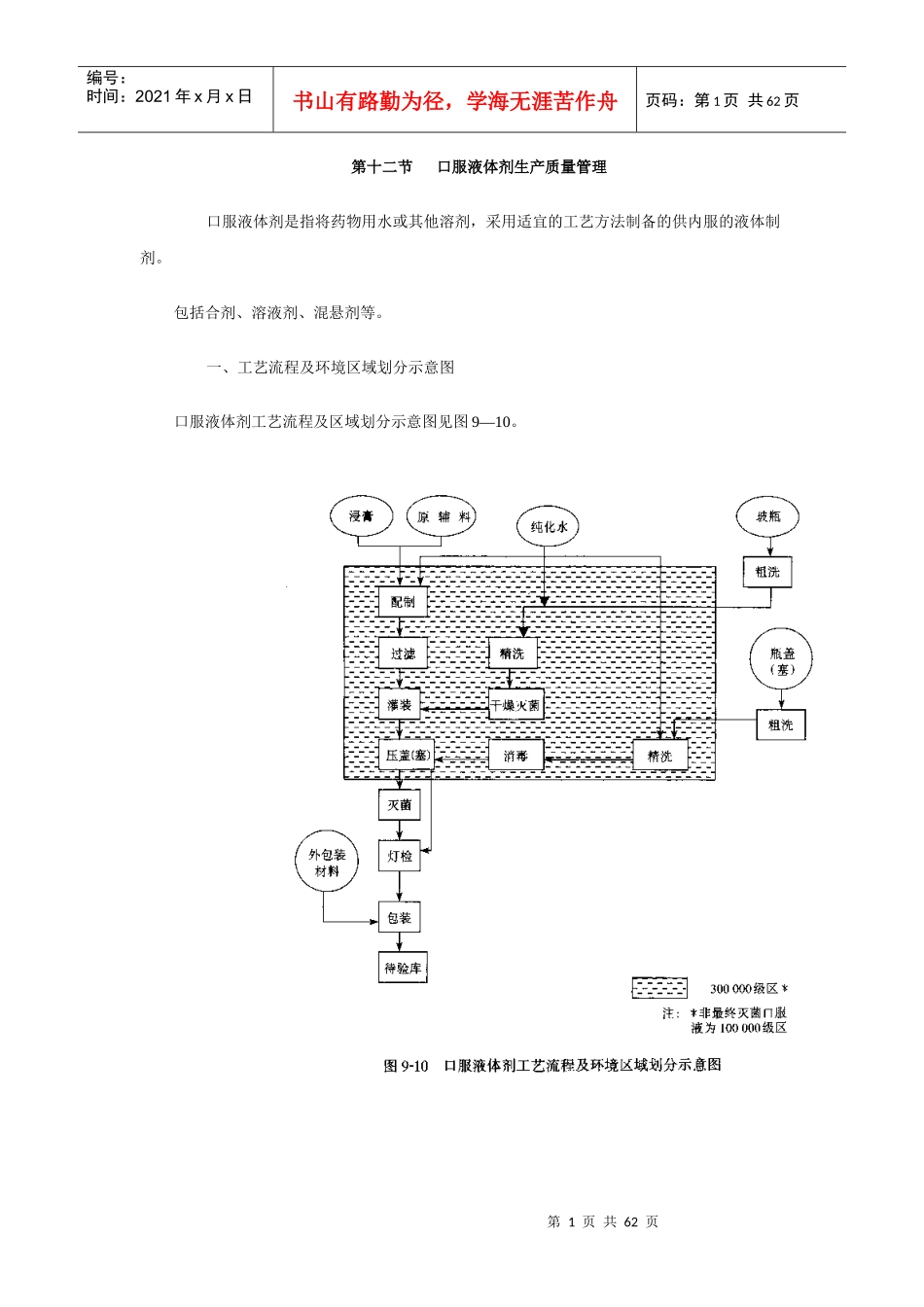
第1页共62页编号:时间:2021年x月x日书山有路勤为径,学海无涯苦作舟页码:第1页共62页第十二节口服液体剂生产质量管理口服液体剂是指将药物用水或其他溶剂,采用适宜的工艺方法制备的供内服的液体制剂。包括合剂、溶液剂、混悬剂等。一、工艺流程及环境区域划分示意图口服液体剂工艺流程及区域划分示意图见图9—10。第2页共62页第1页共62页编号:时间:2021年x月x日书山有路勤为径,学海无涯苦作舟页码:第2页共62页二、生产场所要求(1)口服液体剂因药物性能不同,生产环境的洁净度级别要求也不同。非最终灭菌口服液的暴露工序为100000级;最终灭菌口服液的暴露工序为300000级。(2)各工序应有独立的生产操作间;配备足够的辅助用房。三、设备要求(1)应具备与生产品种相适应的设备,如纯化水处理设备,乳化机、均质机、配料罐、过滤设备、搅拌设备,定量分装机、干燥灭菌设备、高压灭菌柜等。(2)生产设备、容器应有明显的状态标记,标明所加工产品名称、批号等。四、工艺用水配制口服液的工艺用水及直接接触药品的设备、器具和包装材料最后一次洗涤用水应符合《中华人民共和国兽药典》纯化水质量标准。配制用水应使用新制备的纯化水,其贮藏时间不宜超过24h。五、生产管理要点1.生产前的检查(1)检查所生产品种的批生产指令及相应配套文件,记录是否准备齐全。(2)检查本批生产所需的原捕料是否已准备妥当,是否是合格产品。(3)检查设备状况,挂有“合格”、“已清洁”状态标志牌的方可投入使用。(4)是否有清场合格证。(5)对计量器具进行校零,并定期检定。2.生产过程的管理第3页共62页第2页共62页编号:时间:2021年x月x日书山有路勤为径,学海无涯苦作舟页码:第3页共62页(1)称量、配料。①进入备料室的原辅料或中间产品,必须除去外包装或经净化处理。②生产混悬液的原料,其不溶性药物的颗粒度应达到规定要求。③称量人核对原辅料、中间产品的品名、批号、合格证等,确认无误后,按规定的方法和生产指令的定额量称量、记录、签名。④称量必须复核,复核人核对称量后的原辅料、中间产品的品名、数量,确认无误后记录、签名。⑤需计算后称量的原辅料、中间产品,计算结果先经复核无误后再称量。⑥配好的批量原辅料、中间产品装入洁净密闭容器中,附上标志,注明品名、批号、规格、数量、称量人、日期等。⑦剩余原辅料、中间产品包装好,附上标志,放备料室,记录、签名。(2)配制。①口服液配制使用的纯化水,器贮存时间不宜超过24h。②按工艺规程规定的工艺条件进行配制,配制好的药液应作性状、pH、相对密度、定性、定量等质量检验o③口服液中若加附加剂,其品种与用量应符合国家标准的有关规定,不得影响产品的稳定性。④混悬剂中的混悬物应分散均匀,不应很快下沉并不得结块。混悬液的沉降体积比应符合规定。(3)过滤。①按工艺要求选用适宜的滤材和过滤方法。第4页共62页第3页共62页编号:时间:2021年x月x日书山有路勤为径,学海无涯苦作舟页码:第4页共62页②过滤效果应经验证确认。③过滤后药液贮于洁净密闭容器中,通气口应有过滤装置,容器上附有标志,注明品名、规格、批号、数量、操作日期、班次、操作者等.经含量、澄清度等检查合格后方可供灌装用。(4)洗瓶、干燥。①根据瓶子的规格、形状,选用适宜的清洁及清洗方法。粗洗时应洗净瓶子内外壁。②清洗效果经验证确认。③瓶子以纯化水精洗后及时干燥(灭菌),干燥后的瓶子应有防止再污染的措施,瓶子存放时间应经验证确定。④直接接触药液的内塞,用清洁剂,饮用水洗净后,用纯化水精洗,以适宜的消毒方法消毒或以酒精浸泡后使用。(5)灌装、压盖。①先用纯化水冲洗灌装管道,罐装机上的容器、管件、软管应选用不脱落微粒的材质。②开机灌装初期应检查装量,调整至灌装量符合要求后,正式开始灌装操作。③配制好的药液一般应在当天灌装完毕,否则应将药液在规定条件下保存,确保药液不变质。④压盖时检查瓶盖的紧密度,质量符合要求后正式操作。⑤操作过程中随时检查装量和压盖质量,剔除不合格品。⑥中间产品容器中应有标志,注明品名、规格、批号、日期、班次、设备号、操作者等。(6)灭菌。①宜采用双扉式灭菌柜,或...


 VIP
VIP VIP
VIP VIP
VIP VIP
VIP VIP
VIP VIP
VIP VIP
VIP VIP
VIP VIP
VIP VIP
VIP