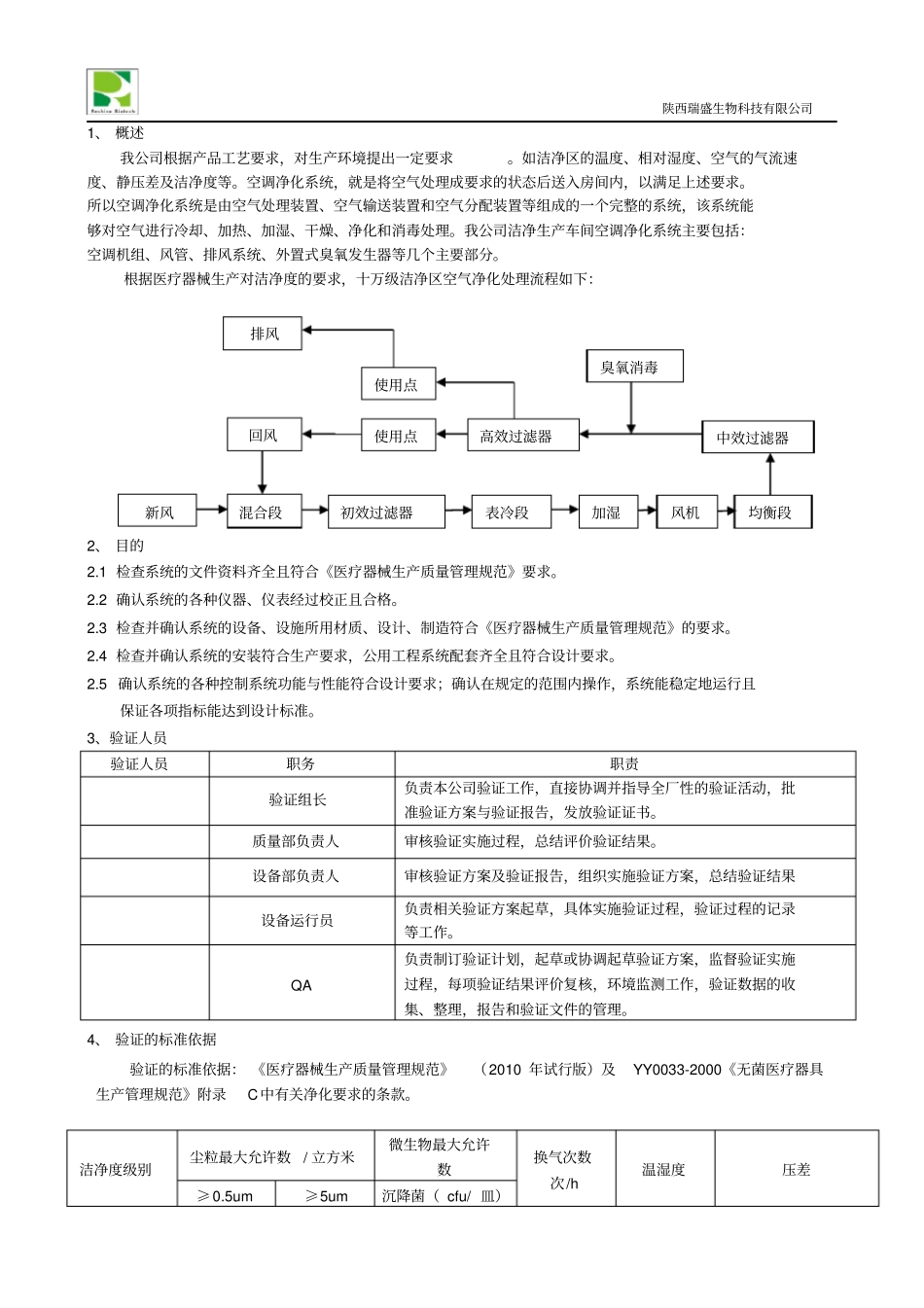
陕西瑞盛生物科技有限公司生产车间空调净化系统再验证报告VR-XT-18001起草人:日期:审核人:日期:批准人:日期:陕西瑞盛生物科技有限公司陕西瑞盛生物科技有限公司目录1、概述2、目的3、验证人员4、验证的标准依据5、验证进度6、验证方案内容6.1验证用仪器仪表的校验6.2安装确认6.3运行确认6.4性能确认6.5日常监测程序及验证周期7、验证总结及结果批准7.1验证总结7.2验证结果审查7.3验证结果批准8、验证报告陕西瑞盛生物科技有限公司1、概述我公司根据产品工艺要求,对生产环境提出一定要求。如洁净区的温度、相对湿度、空气的气流速度、静压差及洁净度等。空调净化系统,就是将空气处理成要求的状态后送入房间内,以满足上述要求。所以空调净化系统是由空气处理装置、空气输送装置和空气分配装置等组成的一个完整的系统,该系统能够对空气进行冷却、加热、加湿、干燥、净化和消毒处理。我公司洁净生产车间空调净化系统主要包括:空调机组、风管、排风系统、外置式臭氧发生器等几个主要部分。根据医疗器械生产对洁净度的要求,十万级洁净区空气净化处理流程如下:2、目的2.1检查系统的文件资料齐全且符合《医疗器械生产质量管理规范》要求。2.2确认系统的各种仪器、仪表经过校正且合格。2.3检查并确认系统的设备、设施所用材质、设计、制造符合《医疗器械生产质量管理规范》的要求。2.4检查并确认系统的安装符合生产要求,公用工程系统配套齐全且符合设计要求。2.5确认系统的各种控制系统功能与性能符合设计要求;确认在规定的范围内操作,系统能稳定地运行且保证各项指标能达到设计标准。3、验证人员验证人员职务职责验证组长负责本公司验证工作,直接协调并指导全厂性的验证活动,批准验证方案与验证报告,发放验证证书。质量部负责人审核验证实施过程,总结评价验证结果。设备部负责人审核验证方案及验证报告,组织实施验证方案,总结验证结果设备运行员负责相关验证方案起草,具体实施验证过程,验证过程的记录等工作。QA负责制订验证计划,起草或协调起草验证方案,监督验证实施过程,每项验证结果评价复核,环境监测工作,验证数据的收集、整理,报告和验证文件的管理。4、验证的标准依据验证的标准依据:《医疗器械生产质量管理规范》(2010年试行版)及YY0033-2000《无菌医疗器具生产管理规范》附录C中有关净化要求的条款。洁净度级别尘粒最大允许数/立方米微生物最大允许数换气次数次/h温湿度压差≥0.5um≥5um沉降菌(cfu/皿)排风表冷段混合段使用点高效过滤器中效过滤器初效过滤器加湿风机使用点臭氧消毒新风均衡段回风陕西瑞盛生物科技有限公司100000级35000002000010≥1518-28℃45-65%不同级别洁净室(区)及洁净室(区)与非洁净室(区)≥5Pa,洁净室(区)与室外大气的静压差应≥10Pa5、验证进度本次验证时限为年月日至年月日。6、验证方案内容6.1验证用仪器仪表的校验在HVAC系统的测试、调整及监控过程中,需要对空气的状态参数、空调设备的性能、房间的洁净度等进行大量的测定工作,将测得的数据与设计数据进行比较、判断,这些物理参数的测定需要通过准确可靠的仪表及仪器来完成。为保证测量数据的准确可靠,必须对仪器、仪表进行校验。安装在设施、设备上的仪器、仪表以及本公司负责进行监测的项目所需仪器、仪表必须进行校验,委托外单位进行监测的项目所需仪器仪表应由监测单位负责对监测用仪器、仪表进行校验。主要校验的仪器有温湿度计、风速仪、压差表、粒子计数器等。将仪器、仪表校验情况记录见附表1。检查结果:检查人:QA:日期:6.2安装确认空调器的安装确认主要是指设备安装后,对照设计图纸及供应商提供的技术资料,检查安装是否符合设计及安装规范。6.2.1确认所需的文件文件名称存放地点检查结果净化空调系统标准操作规程设备部空调间空调机组维护保养标准操作规程设备部空调间空调系统过滤器的清洁更换及消毒灭菌标准操作规程设备部空调间空调机房管理规程设备部空调间洁净区环境监测管理规程质量管理部自动换挡数字式照度计标准操作规程质量管理部智能热球式风速仪标准操作规程质量管理部激光尘埃粒子计数器标准操作规程质量管理部检查人:复核...