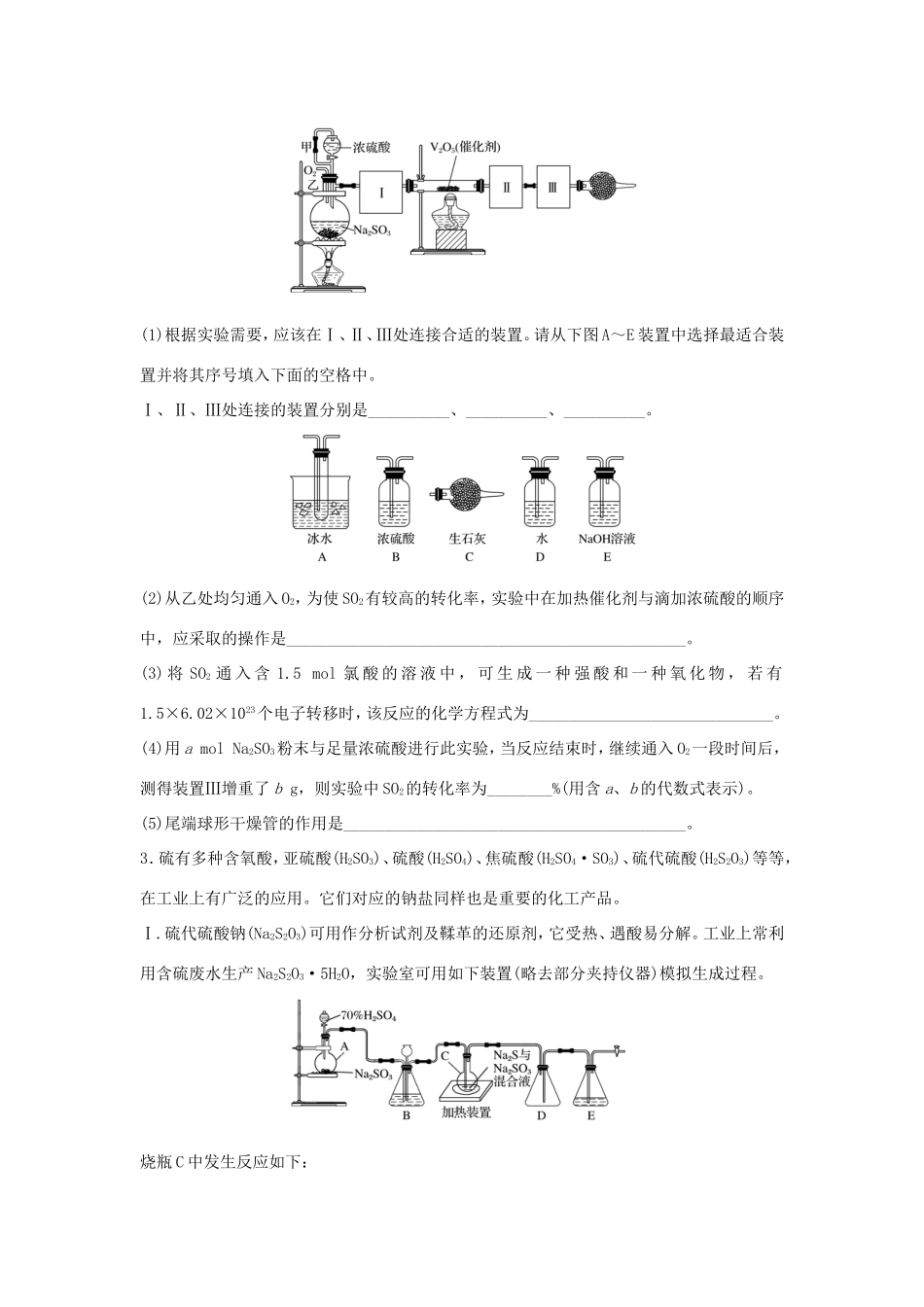
微考点31以硫的转化为核心的探究1.(2017·徐州一中高三调研)某化学兴趣小组利用如图所示装置对SO2的性质进行实验研究。请回答下列问题:(1)装置B的作用是____________。(2)装置C的目的是检验SO2的__________性。装置D中NaOH全部转化为NaHSO3的标志是________________________________________________________________________。(3)向装置D所得NaHSO3溶液中加入漂白粉,有三种可能的情况:Ⅰ.HSO与ClO-刚好反应完Ⅱ.漂白粉不足Ⅲ.漂白粉过量甲同学分别取上述混合溶液于试管中,通过下列实验确定属于哪一种情况,请完成下表。(已知酸性:H2SO4>H2CO3>HClO)实验序号实验操作现象可能的情况①滴加少量淀粉KI溶液,振荡Ⅲ②滴加少量溴水,振荡Ⅱ③滴加少量酸性KMnO4溶液,振荡溶液呈紫色④加入几小块CaCO3固体有气泡产生(4)该小组同学认为,SO2通入含有BaCl2的双氧水中会出现白色沉淀,该反应的离子方程式为________________________________________________________________________________________________________________________________________________。2.(2017·江都一中高三调研)用下图装置可以进行测定SO2转化成SO3的转化率的实验。已知SO3的熔点是16.8℃,沸点是445.8℃。已知发生装置中所涉及反应的化学方程式为Na2SO3(s)+H2SO4(98%)===Na2SO4+H2O+SO2↑。(1)根据实验需要,应该在Ⅰ、Ⅱ、Ⅲ处连接合适的装置。请从下图A~E装置中选择最适合装置并将其序号填入下面的空格中。Ⅰ、Ⅱ、Ⅲ处连接的装置分别是__________、__________、__________。(2)从乙处均匀通入O2,为使SO2有较高的转化率,实验中在加热催化剂与滴加浓硫酸的顺序中,应采取的操作是_________________________________________________。(3)将SO2通入含1.5mol氯酸的溶液中,可生成一种强酸和一种氧化物,若有1.5×6.02×1023个电子转移时,该反应的化学方程式为______________________________。(4)用amolNa2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,测得装置Ⅲ增重了bg,则实验中SO2的转化率为________%(用含a、b的代数式表示)。(5)尾端球形干燥管的作用是__________________________________________。3.硫有多种含氧酸,亚硫酸(H2SO3)、硫酸(H2SO4)、焦硫酸(H2SO4·SO3)、硫代硫酸(H2S2O3)等等,在工业上有广泛的应用。它们对应的钠盐同样也是重要的化工产品。Ⅰ.硫代硫酸钠(Na2S2O3)可用作分析试剂及鞣革的还原剂,它受热、遇酸易分解。工业上常利用含硫废水生产Na2S2O3·5H2O,实验室可用如下装置(略去部分夹持仪器)模拟生成过程。烧瓶C中发生反应如下:Na2S(aq)+H2O(l)+SO2(g)===Na2SO3(aq)+H2S(aq)(Ⅰ)2H2S(aq)+SO2(g)===3S(s)+2H2O(l)(Ⅱ)S(s)+Na2SO3(aq)=====Na2S2O3(aq)(Ⅲ)(1)烧瓶A中发生反应的化学方程式为________________________________,装置D的作用是______________。(2)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择___________(填序号)。a.蒸馏水b.饱和Na2SO3溶液c.饱和NaHSO3溶液d.饱和NaHCO3溶液(3)反应后期可用酒精灯适当加热烧瓶A,实验室用酒精灯加热时必须使用石棉网的仪器还有______(填序号)。a.烧杯b.蒸发皿c.试管d.锥形瓶(4)为了保证硫代硫酸钠的产量,实验中通入SO2不能过量,原因是________________________________________________________________________。Ⅱ.焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。Na2S2O5溶于水即生成NaHSO3。(5)证明NaHSO3溶液中HSO的电离程度大于水解程度,可采用的实验方法是________(填序号)。a.测定溶液的pHb.加入Ba(OH)2溶液c.加入盐酸d.加入品红溶液e.用蓝色石蕊试纸检测(6)葡萄酒常用Na2S2O5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:葡萄酒样品(已知:滴定时反应的化学方程式为SO2+I2+2H2O===H2SO4+2HI)①按上述方案实验,消耗标准I2溶液25.00mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为________g·L-1。②在上述实验过程中,若有部分HI被空气氧化,则测得结果__________(填“偏高”、“偏低”或“不变”)...