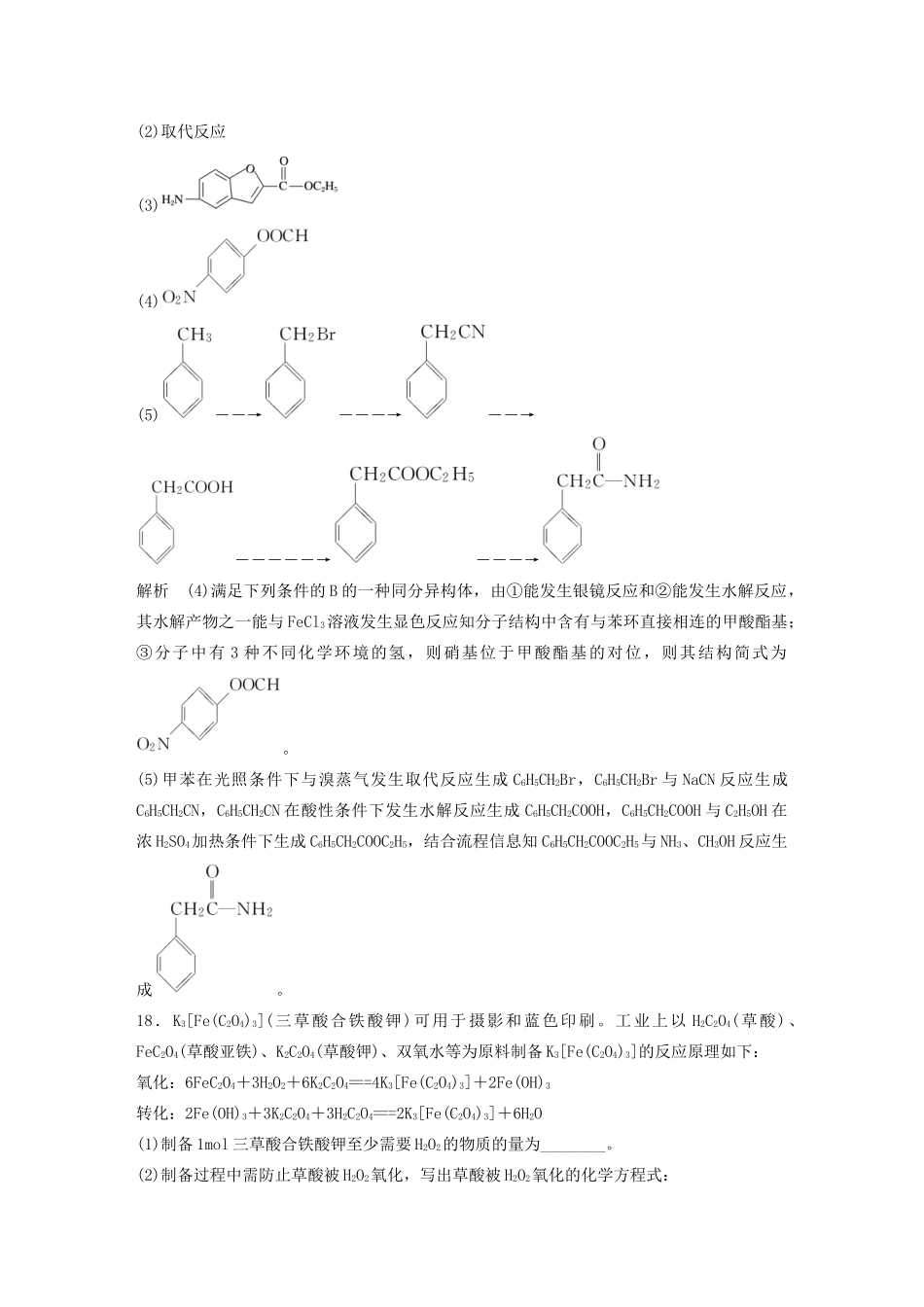
非选择题规范练三16.氧化锂(Li2O)是锂电池工业的重要原料。以粗碳酸锂为原料制备氧化锂的一种工艺流程如下:注:常温下,碳酸锂微溶于水,氢氧化锂可溶于水。(1)反应Ⅰ中通入CO2需加压的原因是__________________________________________。(2)①反应Ⅱ生成LiOH的化学方程式为_________________________________________。②石灰乳的固液比[Ca(OH)2的质量与H2O的体积之比]对LiOH产率和滤液中LiOH浓度的影响如图所示。实际生产中选择的固液比为25g·L-1,若固液比过低对后续操作的不利影响是________________________________________________________________________。(3)浓缩、结晶所得的LiOH·H2O通过灼烧得到Li2O。①LiOH·H2O中常含有少量的Li2CO3,但该物质对所制Li2O的纯度无影响,其原因是________________________________________________________________________________________________________________________________________________。②将LiOH·H2O置于不同坩埚内,在空气中充分灼烧,反应后固体产物的XRD图谱如图所示(XRD图谱可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)。欲制得高纯氧化锂最适宜的坩埚是________________。铁坩埚中发生反应的化学方程式为________________________________________________________________________。答案(1)促进Li2CO3的转化,加快Li2CO3反应的速率(2)①LiHCO3+Ca(OH)2===CaCO3+LiOH+H2O②所得滤液LiOH浓度太低,不利于后期的浓缩结晶(3)①Li2CO3高温分解生成Li2O②锂化刚玉坩埚20LiOH·H2O+4Fe+3O2=====4Li5FeO4+30H2O解析(1)反应Ⅰ中碳酸锂悬浊液与二氧化碳反应生成LiHCO3,通入CO2时,加压可以促进Li2CO3的转化,加快Li2CO3反应的速率。(2)②根据石灰乳的固液比[Ca(OH)2的质量与H2O的体积之比]对LiOH产率和滤液中LiOH浓度的影响可知,实际生产中选择固液比为25g·L-1,若固液比过低,所得滤液LiOH浓度太低,不利于后期的浓缩结晶。(3)②将LiOH·H2O置于不同坩埚内,在空气中充分灼烧,根据反应后固体产物的XRD图谱可知,欲制得高纯氧化锂最适宜的坩埚是锂化刚玉坩埚,在铁坩埚中LiOH·H2O受热反应得到Li5FeO4,反应的方程式为20LiOH·H2O+4Fe+3O2=====4Li5FeO4+30H2O。17.维拉佐酮是临床上广泛使用的抗抑郁药,其关键中间体的合成路线如下:(1)D中的含氧官能团名称为______________________(任写两种)。(2)B→C的反应类型为__________________________________________。(3)化合物E的结构简式为________________________________________。(4)写出同时满足下列条件的B的一种同分异构体的结构简式:__________。①能发生银镜反应;②能发生水解反应,其水解产物之一能与FeCl3溶液发生显色反应;③分子中有3种不同化学环境的氢。(5)已知:RBr――→RCN――→RCOOH。请以甲苯和乙醇为原料制备,写出相应的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。答案(1)硝基、酯基、醚键(任写两种即可)(2)取代反应(3)(4)(5)――→―――→――→―――――→―――→解析(4)满足下列条件的B的一种同分异构体,由①能发生银镜反应和②能发生水解反应,其水解产物之一能与FeCl3溶液发生显色反应知分子结构中含有与苯环直接相连的甲酸酯基;③分子中有3种不同化学环境的氢,则硝基位于甲酸酯基的对位,则其结构简式为。(5)甲苯在光照条件下与溴蒸气发生取代反应生成C6H5CH2Br,C6H5CH2Br与NaCN反应生成C6H5CH2CN,C6H5CH2CN在酸性条件下发生水解反应生成C6H5CH2COOH,C6H5CH2COOH与C2H5OH在浓H2SO4加热条件下生成C6H5CH2COOC2H5,结合流程信息知C6H5CH2COOC2H5与NH3、CH3OH反应生成。18.K3[Fe(C2O4)3](三草酸合铁酸钾)可用于摄影和蓝色印刷。工业上以H2C2O4(草酸)、FeC2O4(草酸亚铁)、K2C2O4(草酸钾)、双氧水等为原料制备K3[Fe(C2O4)3]的反应原理如下:氧化:6FeC2O4+3H2O2+6K2C2O4===4K3[Fe(C2O4)3]+2Fe(OH)3转化:2Fe(OH)3+3K2C2O4+3H2C2O4===2K3[Fe(C2O4)3]+6H2O(1)制备1mol三草酸合铁酸钾至少需要H2O2的物质的量为________。(2)制备过程中需防止草酸被H2O2氧化,写出草...