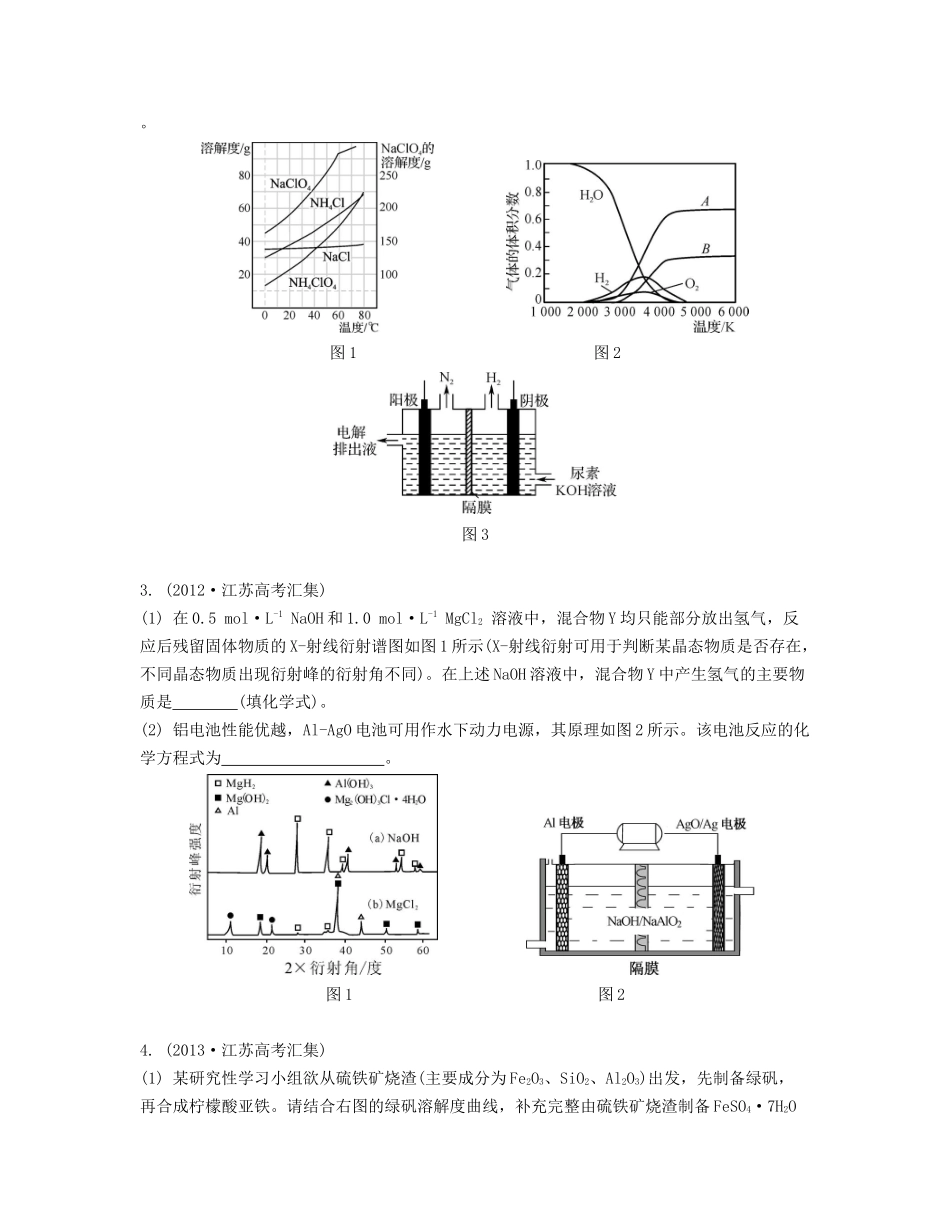
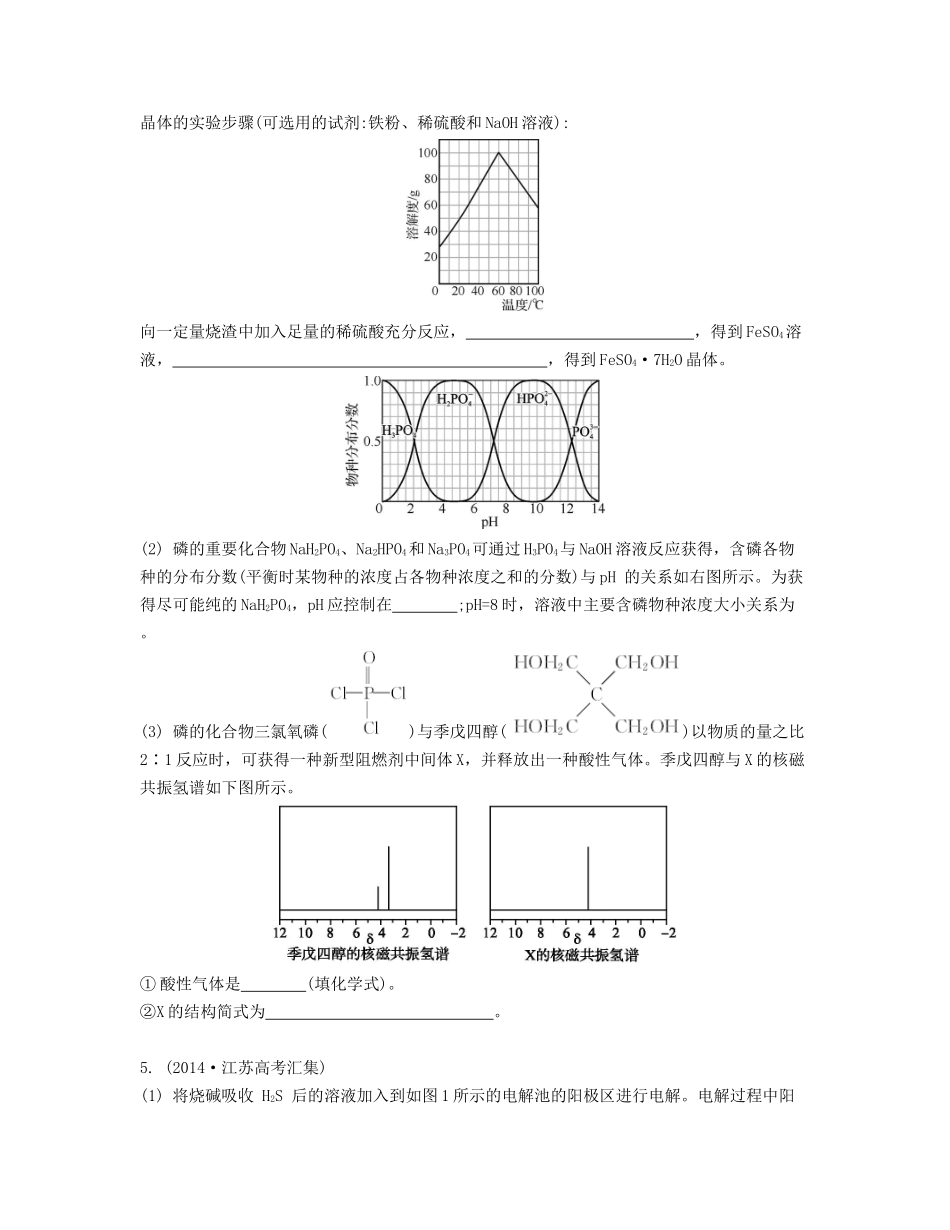
专题十考前回归(化学识图)1.(2012·江苏高考汇集)(1)若实验中将N2换成空气,测得反应液中Mn2+、S的浓度(c)随反应时间(t)的变化如图1所示。导致溶液中Mn2+、S的浓度变化产生明显差异的原因是。(2)方法Ⅲ中用惰性电极电解NaHSO3溶液的装置如图2所示。阳极区放出气体的成分为(填化学式)。(3)Co(OH)2在空气中加热时,固体残留率随温度的变化如图3所示。已知钴的氢氧化物加热至290℃时已完全脱水,则1000℃时,剩余固体的成分为;在350400℃范围内,剩余固体的成分为。(填化学式)图1图2图32.(2011·江苏高考汇集)(1)反应得到的混合溶液中NH4ClO4和NaCl的质量分数分别为0.30和0.15(相关物质的溶解度曲线见图1)。从混合溶液中获得较多NH4ClO4晶体的实验操作依次为(填操作名称)、干燥。(2)H2O的热分解也可得到H2,高温下水分解体系中主要气体的体积分数与温度的关系如图2所示。图中A、B表示的依次是。(3)电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图见图3(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。电解时,阳极的电极反应式为2-4O2-4O。图1图2图33.(2012·江苏高考汇集)(1)在0.5mol·L-1NaOH和1.0mol·L-1MgCl2溶液中,混合物Y均只能部分放出氢气,反应后残留固体物质的X-射线衍射谱图如图1所示(X-射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)。在上述NaOH溶液中,混合物Y中产生氢气的主要物质是(填化学式)。(2)铝电池性能优越,Al-AgO电池可用作水下动力电源,其原理如图2所示。该电池反应的化学方程式为。图1图24.(2013·江苏高考汇集)(1)某研究性学习小组欲从硫铁矿烧渣(主要成分为Fe2O3、SiO2、Al2O3)出发,先制备绿矾,再合成柠檬酸亚铁。请结合右图的绿矾溶解度曲线,补充完整由硫铁矿烧渣制备FeSO4·7H2O晶体的实验步骤(可选用的试剂:铁粉、稀硫酸和NaOH溶液):向一定量烧渣中加入足量的稀硫酸充分反应,,得到FeSO4溶液,,得到FeSO4·7H2O晶体。(2)磷的重要化合物NaH2PO4、Na2HPO4和Na3PO4可通过H3PO4与NaOH溶液反应获得,含磷各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系如右图所示。为获得尽可能纯的NaH2PO4,pH应控制在;pH=8时,溶液中主要含磷物种浓度大小关系为。(3)磷的化合物三氯氧磷()与季戊四醇()以物质的量之比2∶1反应时,可获得一种新型阻燃剂中间体X,并释放出一种酸性气体。季戊四醇与X的核磁共振氢谱如下图所示。①酸性气体是(填化学式)。②X的结构简式为。5.(2014·江苏高考汇集)(1)将烧碱吸收H2S后的溶液加入到如图1所示的电解池的阳极区进行电解。电解过程中阳极区发生如下反应:S2--2e-S、(n-1)S+S2-。①写出电解时阴极的电极反应式:。②电解后阳极区的溶液用稀硫酸酸化得到硫单质,其离子方程式可写成。(2)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应回收S,其物质转化如图2所示。在图示的转化中,化合价不变的元素是。(3)H2S在高温下分解生成硫蒸气和H2。若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如图3所示,H2S在高温下分解反应的化学方程式为。图1图2图36.(2014·盐城期中)图1(1)高氯酸铵可用于火箭推进剂,实验室可由NaClO3等原料制取(部分物质溶解度如图1),2-Sn其实验流程如下:①氯酸钠受热分解生成高氯酸钠和氯化钠的化学方程式为。②80℃时浸取液冷却至0℃过滤,滤渣的主要成分为(填化学式)。(2)某化学课外小组拟用废旧干电池锌皮(含杂质铁),结合图2信息利用实验可提供的试剂制取纯净的ZnSO4溶液。图2实验中可选用的试剂如下:(a)30%H2O2;(b)新制氯水;(c)1.0mol·NaOH溶液;(d)3mol·L-1稀硫酸;(e)纯ZnO粉末;(f)纯锌粉。实验步骤依次为:①将锌片完全溶于稍过量的3mol·稀硫酸,加入(填字母,下同);②加入;③加热到60℃左右并不断搅拌;④过滤得ZnSO4溶液。其中步骤③加热的主要目的有。图3(3)氯化铜溶液中铜各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与c(Cl-)的关系如图3所示。①当c(Cl-)=9mol·时,溶液中主要的3种含铜物种浓度大小关系为。-1L-1L-1L②在c(Cl-)=1mol·的氯化铜溶液中,滴入AgNO3溶液,含铜物种间转化的...