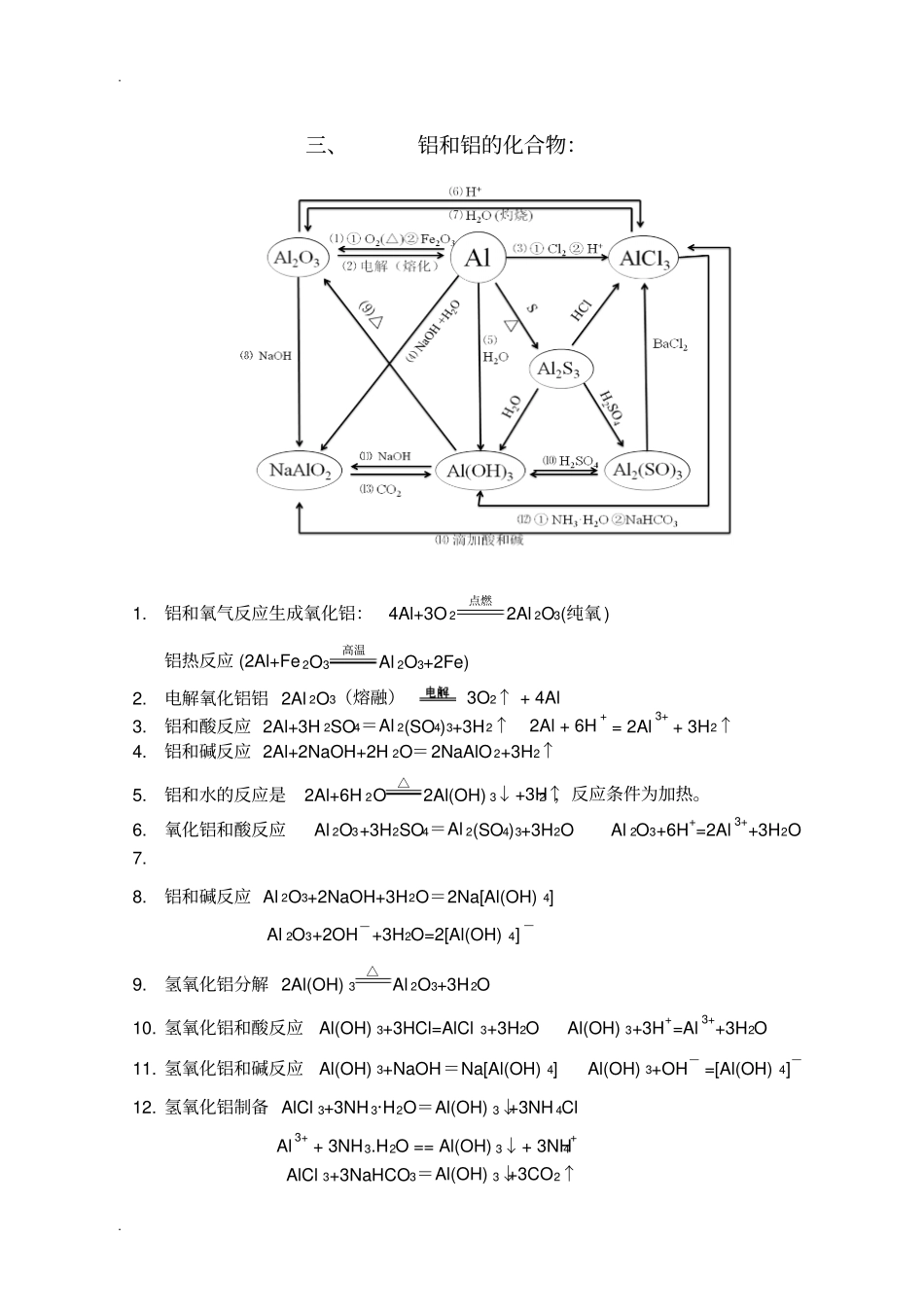
..必修一化学方程式一.过量1.澄清石灰水中通入少量二氧化碳:Ca(OH)2+CO2══CaCO3+H2O2.澄清石灰水中通入过量二氧化碳Ca(OH)2+2CO2══Ca(HCO3)23.氢氧化钠溶液中通入少量二氧化碳:2NaOH+CO2====Na2CO3+H2O4.氢氧化钠溶液中通入过量二氧化碳;CO2+NaOH====NaHCO35.碳酸钠溶液中加入少量盐酸:Na2CO3+HCl====NaHCO3+NaCl6.碳酸钠溶液中加入足量盐酸:NaHCO3+HCl====NaCl+H2O+CO2↑7.硫酸氢纳溶液中加入少量氢氧化钡:2NaHSO4+Ba(OH)2====BaSO4↓+NaSO4+2H2O8.硫酸氢纳溶液中加入过量的氢氧化钡:NaHSO4+Ba(OH)2====BaSO4↓+NaOH+H2O9.碳酸氢钙溶液中加入少量氢氧化钠溶:Ca(HCO3)2+NaOH===NaHCO3+CaCO3↓+H2O10.碳酸氢钙溶液中加入足量氢氧化钠溶:2NaOH+Ca(HCO3)2=CaCO3↓+2H2O+Na2CO311.澄清石灰水中加入少量的碳酸氢钠溶液:NaHCO3+Ca(OH)2===NaOH+H2O+CaCO3↓12.澄清石灰水中加入少量的碳酸氢钠液:2NaHCO3+Ca(OH)2=Na2CO3+2H2O+CaCO3↓二、钠及其化合物1.钠在空气中燃烧:4Na+O2=2Na2O2.钠在氧气中加热:2Na+O2点燃Na2O2Cl2+2Na点燃2NaCl3.钠与水反应:2Na+2H2O=2NaOH+H2↑2Na+2H2O==2Na++2OH-+H2↑4.钠与硫酸铜溶液反应:2Na+2H2O+CuSO4=Cu(OH)2↓+Na2SO4+H2↑5.钠和氯化铁溶液反应:6Na+6H2O+2FeCl3=2Fe(OH)3↓+6NaCl+3H2↑6.氧化钠的主要化学性质:2Na2O+O2△2Na2O2Na2O+H2O=2NaOHNa2O+SO3=Na2SO4Na2O+CO2=Na2CO3Na2O+2HCl=2NaCl+H2O7.过氧化钠与水反应:2Na2O2+2H2O=4NaOH+O2↑8.过氧化钠与二氧化碳反应:2Na2O2+2CO2=2Na2CO3+O29.过氧化钠和硫酸反应:Na2O2+H2SO4(冷、稀)=Na2SO4+H2O210.过氧化钠和二氧化硫反应Na2O2+SO2=Na2SO411.土法制烧碱:Ca(OH)2+Na2CO2=CaCO3↓+2NaOH12.二氧化碳通入饱和碳酸钠溶液:Na2CO3+H2O+CO2=2NaHCO3↓13.碳酸氢钠受热分解:2NaHCO3===Na2CO3+H2O+CO2↑..三、铝和铝的化合物:1.铝和氧气反应生成氧化铝:4Al+3O2点燃2Al2O3(纯氧)铝热反应(2Al+Fe2O3高温Al2O3+2Fe)2.电解氧化铝铝2Al2O3(熔融)3O2↑+4Al3.铝和酸反应2Al+3H2SO4=Al2(SO4)3+3H2↑2Al+6H+=2Al3++3H2↑4.铝和碱反应2Al+2NaOH+2H2O=2NaAlO2+3H2↑5.铝和水的反应是2Al+6H2O△2Al(OH)3↓+3H2↑,反应条件为加热。6.氧化铝和酸反应Al2O3+3H2SO4=Al2(SO4)3+3H2OAl2O3+6H+=2Al3++3H2O7.8.铝和碱反应Al2O3+2NaOH+3H2O=2Na[Al(OH)4]Al2O3+2OH—+3H2O=2[Al(OH)4]—9.氢氧化铝分解2Al(OH)3△Al2O3+3H2O10.氢氧化铝和酸反应Al(OH)3+3HCl=AlCl3+3H2OAl(OH)3+3H+=Al3++3H2O11.氢氧化铝和碱反应Al(OH)3+NaOH=Na[Al(OH)4]Al(OH)3+OH—=[Al(OH)4]—12.氢氧化铝制备AlCl3+3NH3·H2O=Al(OH)3↓+3NH4ClAl3++3NH3.H2O==Al(OH)3↓+3NH4+AlCl3+3NaHCO3=Al(OH)3↓+3CO2↑..Al3++3HCO3-==Al(OH)3↓+3CO2↑13.偏铝酸钠溶液中通入二氧化碳(少量、过量)2NaAlO2+3H2O+CO2=2Al(OH)3↓+Na2CO3Na2CO3+H2O+CO2=2NaHCO3NaAlO2+2H2O+CO2=Al(OH)3↓+NaHCO314.氯化铝中滴入过量的氢氧化钠:AlCl3+4NaOH=NaAlO2+3NaCl+2H2O氢氧化钠溶液滴入过量氯化铝:AlCl3+4NaOH=NaAlO2+3NaCl+2H2O3NaAlO2+AlCl3+6H2O=3NaCl+4Al(OH)3↓偏铝酸钠溶液中滴入过量盐酸:NaAlO2+4HCl=NaCl+AlCl3+2H2O盐酸中滴入过量的偏铝酸钠溶液:NaAlO2+4HCl=NaCl+AlCl3+2H2O3NaAlO2+AlCl3+6H2O=3NaCl+4Al(OH)3↓..四、铁和铁的化合物1.铁在干燥空气中氧化3Fe+2O2点燃Fe3O42.铁和非金属反应2Fe+3Cl2点燃2FeCl3Fe+S△FeS3.铁和水蒸气反应3Fe+4H2O(g)高温Fe3O4+4H24.铁和盐酸反应Fe+2HCl=FeCl2+H2↑Fe+2H+=Fe2++H2↑5.铁的置换Fe+CuSO4=FeSO4+CuFe+Cu2+=Fe2++Cu6.铁被氧化:7.氢氧化亚铁被氧化4Fe(OH)2+O2+2H2O==4Fe(OH)38.氢氧化铁分解2Fe(OH)3△Fe2O3+3H2O9.Fe2+——Fe3+的转化加氧化剂:FeCl2+Cl2=2FeCl310.Fe3+——Fe2+的转化加还原剂:2FeCl3+Fe=3FeCl22FeCl3+Cu=2FeCl2+CuCl2Fe+2Fe3+==3Fe2+2Fe3++Cu==2Fe2++Cu2+11.Fe3+的检验FeCl3+3KSCN==Fe(SCN)3+3KClFe3++3SCN-==Fe(SCN)3(红色溶液)..五、硅及其化合物主要化学性质:1.工业制硅2C+SiO2△Si+2CO(制得粗硅)Si(粗)+2Cl2△SiCl4Si(粉)+O2△SiO2SiCl4+2H2△Si(纯)...