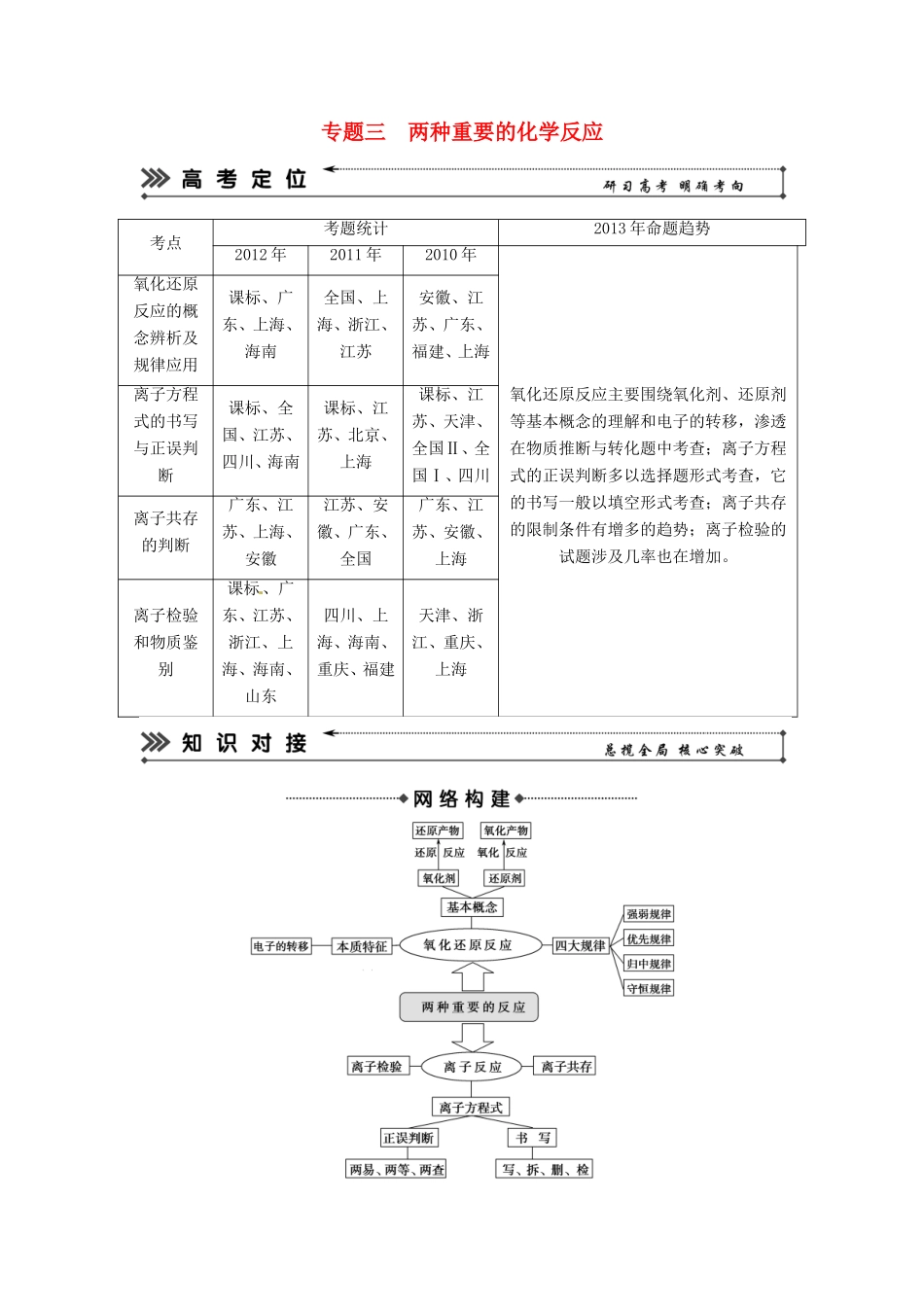
专题三两种重要的化学反应考点考题统计2013年命题趋势2012年2011年2010年氧化还原反应主要围绕氧化剂、还原剂等基本概念的理解和电子的转移,渗透在物质推断与转化题中考查;离子方程式的正误判断多以选择题形式考查,它的书写一般以填空形式考查;离子共存的限制条件有增多的趋势;离子检验的试题涉及几率也在增加。氧化还原反应的概念辨析及规律应用课标、广东、上海、海南全国、上海、浙江、江苏安徽、江苏、广东、福建、上海离子方程式的书写与正误判断课标、全国、江苏、四川、海南课标、江苏、北京、上海课标、江苏、天津、全国Ⅱ、全国Ⅰ、四川离子共存的判断广东、江苏、上海、安徽江苏、安徽、广东、全国广东、江苏、安徽、上海离子检验和物质鉴别课标、广东、江苏、浙江、上海、海南、山东四川、上海、海南、重庆、福建天津、浙江、重庆、上海1.氧化还原反应的概念及电子转移。2.离子方程式的书写和正误判断。3.离子共存的限制条件。4.离子检验的干扰因素。1.氧化还原反应中的四大规律的内涵是什么?答案氧化还原反应中有强弱规律、优先规律、归中规律和守恒规律四大规律。(1)强弱规律是指氧化性较强的氧化剂和还原性较强的还原剂反应生成氧化性较弱的氧化产物和还原性较弱的还原产物,该规律主要用于比较物质间的氧化性或还原性的强弱以及判断氧化还原反应发生的可能性,即“氧化性:氧化剂>氧化产物、还原性:还原剂>还原产物”。(2)优先规律是指当几个氧化还原反应均可能发生时,氧化性或还原性强的粒子优先反应。(3)归中规律是指同一元素不同价态间发生氧化还原反应时,高价态+低价态=中间价态,即“只靠拢,不交叉”,此规律可用于判断物质氧化性与还原性及判断反应中的氧化剂、还原剂、还原产物、氧化产物。(4)守恒规律是指氧化还原反应中变价元素的化合价升高总数与降低总数相等,或变价元素得到电子总数与失去的电子总数相等,该规律主要用于化学计算和氧化还原反应化学方程式的配平。2.离子反应的条件有哪些?答案离子反应的条件有:(1)生成沉淀、(2)生成气体、(3)生成弱电解质、(4)发生氧化还原反应、(5)发生相互促进的水解反应、(6)发生络合反应等。3.离子方程式的正误判断的“两易、两等、两查”分别指什么?答案离子方程式的正误判断中的“两易”是易溶、易电离的物质(即可溶的强电解质,包括强酸、强碱、大多数可溶性的盐)以实际参加反应的离子符号表示,非电解质、弱电解质、难溶物、气体等用化学式表示;“两等”是离子方程式两边的原子个数、电荷总数均应相等;“两查”检查各项化学计量数是否有公约数,是否漏写必要的反应条件。4.常见的阴、阳离子是怎样检验的?答案常见的阴、阳离子的检验(1)常见几种阳离子的检验:Fe3+加NaOH产生红褐色沉淀,加KSCN溶液变血红色;Fe2+加NaOH产生白色沉淀立即变成灰绿色最终变成红褐色,加KSCN无现象再加氯水溶液变红色;NH加OH—并加热,有使润湿的红色石蕊试纸变蓝的气体产生或遇蘸有浓盐酸的玻璃棒有白烟的气体产生;Ba2+加入含有SO的溶液产生不溶于稀HNO3的白色沉淀;Ag+加含有Cl-的溶液产生不溶于稀HNO3的白色沉淀。(2)常见几种阴离子的检验:SO加CaCl2溶液产生白色沉淀(避免HSO的干扰),再加稀盐酸有气体产生,并能使品红褪色;CO加CaCl2溶液产生白色沉淀(避免HCO的干扰),再加稀盐酸有使石灰水变浑浊无色无味的气体产生;Br-加AgNO3溶液产生不溶于稀HNO3的淡黄色沉淀,或滴加氯水、苯或CCl4,溶液分层,苯层或CCl4层橙红色;I-加AgNO3溶液产生不溶于稀HNO3的黄色沉淀,或滴加氯水、苯或CCl4,溶液分层,苯层或CCl4层紫红色,或滴入新制氯水,振荡后再滴入淀粉溶液,变蓝。考点一氧化还原反应的概念辨析及规律应用通过近三年的高考试题看出,氧化还原反应的考查主要集中在氧化剂、还原剂、氧化产物、还原产物等概念的辨析以及氧化还原反应规律的应用。【典例1】(2012·上海,20)火法炼铜首先要焙烧黄铜矿,其反应为:2CuFeS2+O2===Cu2S+2FeS+SO2,下列说法正确的是()。A.SO2既是氧化产物又是还原产物B.CuFeS2仅作还原剂,硫元素被氧化C.每生成1molCu2S,有4mol硫被氧化D.每转移1.2m...