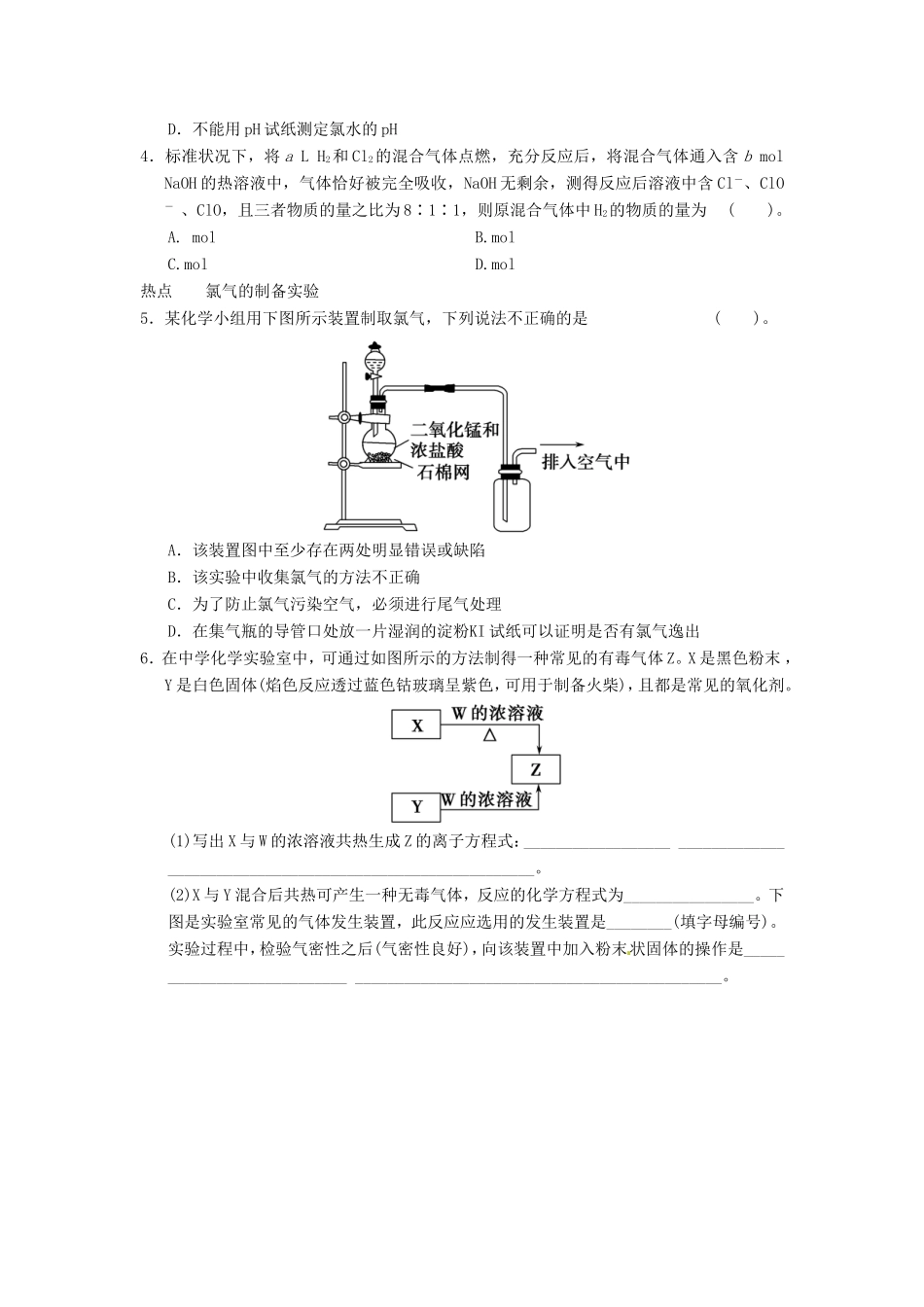
热点狂练十一氯元素的3个热点问题命题热点①氯水的成分与漂白原理②氯气的重要化学性质③氯气的制备实验命题预测卤素是安徽高考的重点内容,对本部分知识单独考查的题目较少,常与其他非金属元素、金属元素等知识结合考查,考查题型有选择题和非选择题。【押题11】下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是()。A.将NaHCO3固体加入新制氯水,有无色气泡产生(H+)B.使红色布条褪色(HCl)C.向FeCl2溶液中滴加氯水,再滴加KSCN溶液,发现呈红色(Cl2)D.滴加AgNO3溶液生成白色沉淀(Cl-)解析氯水使红色布条褪色是因为氯水中存在HClO,而不是因为氯水中存在HCl。答案B1.氯水的成分。新制氯水是含Cl2、HCl、HClO三种溶质的混合溶液,溶液中含有三种分子——H2O、Cl2和HClO,还含有四种离子——H+、Cl-、ClO-和极少量OH-。2.氯水的多重性。①提供H+,体现酸性。②提供Cl-,能与Ag+反应生成沉淀。③提供Cl2分子,使氯水呈黄绿色和表现强氧化性,如2FeCl2+Cl2===2FeCl3。④提供HClO,如用氯水杀菌、消毒、漂白物质。⑤氯水性质的多重性:如氯水能使石蕊试液先变红后褪色(先变红是由于氯水中HCl的酸性;后褪色是由于氯水中HClO的强氧化性)。热点狂练热点氯水的成分与漂白原理1.在氯水中存在多种分子和离子,它们在不同的反应中表现各自的性质。下列实验现象和结论一致且正确的是()。A.向氯水中加入有色布条,一会儿有色布条褪色,说明溶液中有Cl2存在B.溶液呈黄绿色,且有刺激性气味,说明有Cl2分子存在C.先加入盐酸酸化,再加入AgNO3溶液产生白色沉淀,说明溶液中有Cl-存在D.加入NaOH溶液,氯水黄绿色消失,说明有HClO分子存在2.某同学向一支空试管中按一定的顺序分别加入下列四种物质(一种物质只加一次):①KI溶液②淀粉溶液③NaOH溶液④新制氯水。发现溶液颜色按如下顺序变化:无色→棕黄色→蓝色→无色。依据溶液颜色的变化判断加入以上物质的顺序是()。A.①→②→③→④B.①→④→②→③C.②→④→①→③D.①→②→④→③热点氯气的重要化学性质3.下列有关氯元素单质及化合物性质的说法正确的是()。A.液氯是纯净物,氯水是电解质,漂白粉是混合物B.氯气可用作消毒剂和漂白剂,是因为氯分子具有强氧化性C.随着化合价的升高,氯的含氧酸酸性和氧化性均逐渐增强D.不能用pH试纸测定氯水的pH4.标准状况下,将aLH2和Cl2的混合气体点燃,充分反应后,将混合气体通入含bmolNaOH的热溶液中,气体恰好被完全吸收,NaOH无剩余,测得反应后溶液中含Cl-、ClO-、ClO,且三者物质的量之比为8∶1∶1,则原混合气体中H2的物质的量为()。A.molB.molC.molD.mol热点氯气的制备实验5.某化学小组用下图所示装置制取氯气,下列说法不正确的是()。A.该装置图中至少存在两处明显错误或缺陷B.该实验中收集氯气的方法不正确C.为了防止氯气污染空气,必须进行尾气处理D.在集气瓶的导管口处放一片湿润的淀粉KI试纸可以证明是否有氯气逸出6.在中学化学实验室中,可通过如图所示的方法制得一种常见的有毒气体Z。X是黑色粉末,Y是白色固体(焰色反应透过蓝色钴玻璃呈紫色,可用于制备火柴),且都是常见的氧化剂。(1)写出X与W的浓溶液共热生成Z的离子方程式:____________________________________________________________________________。(2)X与Y混合后共热可产生一种无毒气体,反应的化学方程式为________________。下图是实验室常见的气体发生装置,此反应应选用的发生装置是________(填字母编号)。实验过程中,检验气密性之后(气密性良好),向该装置中加入粉末状固体的操作是________________________________________________________________________。(3)Z与乙烯加成可得一种有机物,为验证该有机物中含有与Z相同的元素,请选择合适的试剂________(用字母编号回答)。a.稀盐酸b.稀硝酸c.稀硫酸d.氢氧化钠溶液e.硝酸银溶液f.淀粉溶液g.碘化钾溶液h.品红溶液(4)在实验室中制取气体Z时,通常可用排某种溶液的方法收集Z,则该溶液是________;也可用排空气集气法收集Z,若用右图装置(不能改变瓶口朝向),则气体应该从________(填“m”或“n”...