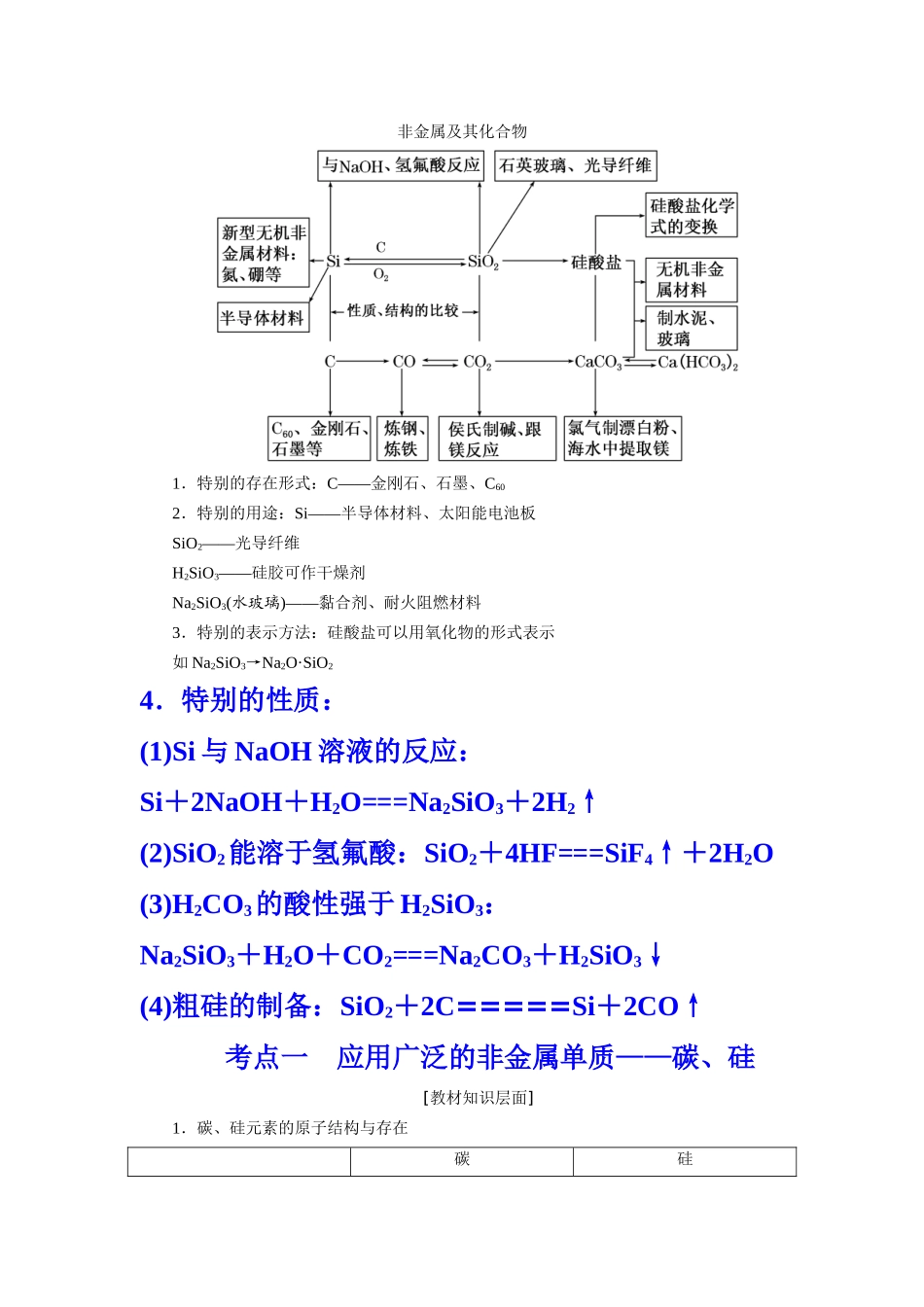
非金属及其化合物1.特别的存在形式:C——金刚石、石墨、C602.特别的用途:Si——半导体材料、太阳能电池板SiO2——光导纤维H2SiO3——硅胶可作干燥剂Na2SiO3(水玻璃)——黏合剂、耐火阻燃材料3.特别的表示方法:硅酸盐可以用氧化物的形式表示如 Na2SiO3→Na2O·SiO24.特别的性质:(1)Si 与 NaOH 溶液的反应:Si+2NaOH+H2O===Na2SiO3+2H2↑(2)SiO2能溶于氢氟酸:SiO2+4HF===SiF4↑+2H2O(3)H2CO3的酸性强于 H2SiO3:Na2SiO3+H2O+CO2===Na2CO3+H2SiO3↓(4)粗硅的制备:SiO2+2C=====Si+2CO↑考点一 应用广泛的非金属单质——碳、硅[教材知识层面]1.碳、硅元素的原子结构与存在碳硅原子结构示意图在元素周期表中的位置第二周期Ⅳ A 族第三周期Ⅳ A 族单质的结构金刚石:空间网状结构石墨:层状结构晶体硅:与金刚石类似的空间网状结构元素在自然界中的存在形式既有游离态又有化合态只有化合态2.碳、硅单质的性质(1)碳、硅的物理性质和用途(用短线连接起来):(提示:①—c,②—a,③—e,④—b,⑤—d)(2)碳、硅的化学性质:① 碳单质的化学性质——还原性。a.与 O2的反应(用化学方程式表示):O2 不足: 2C + O 2 点燃 ,2CO ;O2 充足: C + O 2 点燃 ,CO 2。b.与其他物质的反应(用化学方程式表示):与 CuO 反应:2CuO + C 高温 ,2Cu + CO 2↑(可用于金属的冶炼);与 CO2反应:CO2+ C 高温 ,2CO ;与水蒸气反应:C + H 2O(g) 高温 ,CO + H 2( 制水煤气 ) ;与浓硫酸反应:C + 2H 2SO4( 浓 ) △ ,CO 2↑ + 2SO 2↑ + 2H2O。② 硅的化学性质——还原性。a.与氢氟酸反应的化学方程式:Si + 4HF == =SiF 4↑ + 2H 2↑;b.与 NaOH 溶液反应的化学方程式:Si + 2NaOH + H 2O == =Na 2SiO3+ 2H 2↑;c.与 O2反应:Si + O 2△ ,SiO 2。[高考考查层面]命题点 1 硅单质的特性非金属的一般规律硅的特性硅还原性强于碳2C+SiO2=====Si+2CO↑非金属与强碱溶液反应一般不产生 H2硅可与强碱溶液反应产生 H2:Si+2NaOH+H2O===Na2SiO3+2H2↑非金属一般不与非氧化性酸反应Si+4HF===SiF4↑+2H2↑一般非金属单质为绝缘体硅为半导体,常用于电子部件[典题示例]推断下列描述的正误(正确的打“√”,错误的打“×”)。(1)(2024·广东高考)高温下用焦炭还原 SiO2 制取粗硅 ()(2)单质硅是将太阳能转变为电能的常用材料 ()(3)...