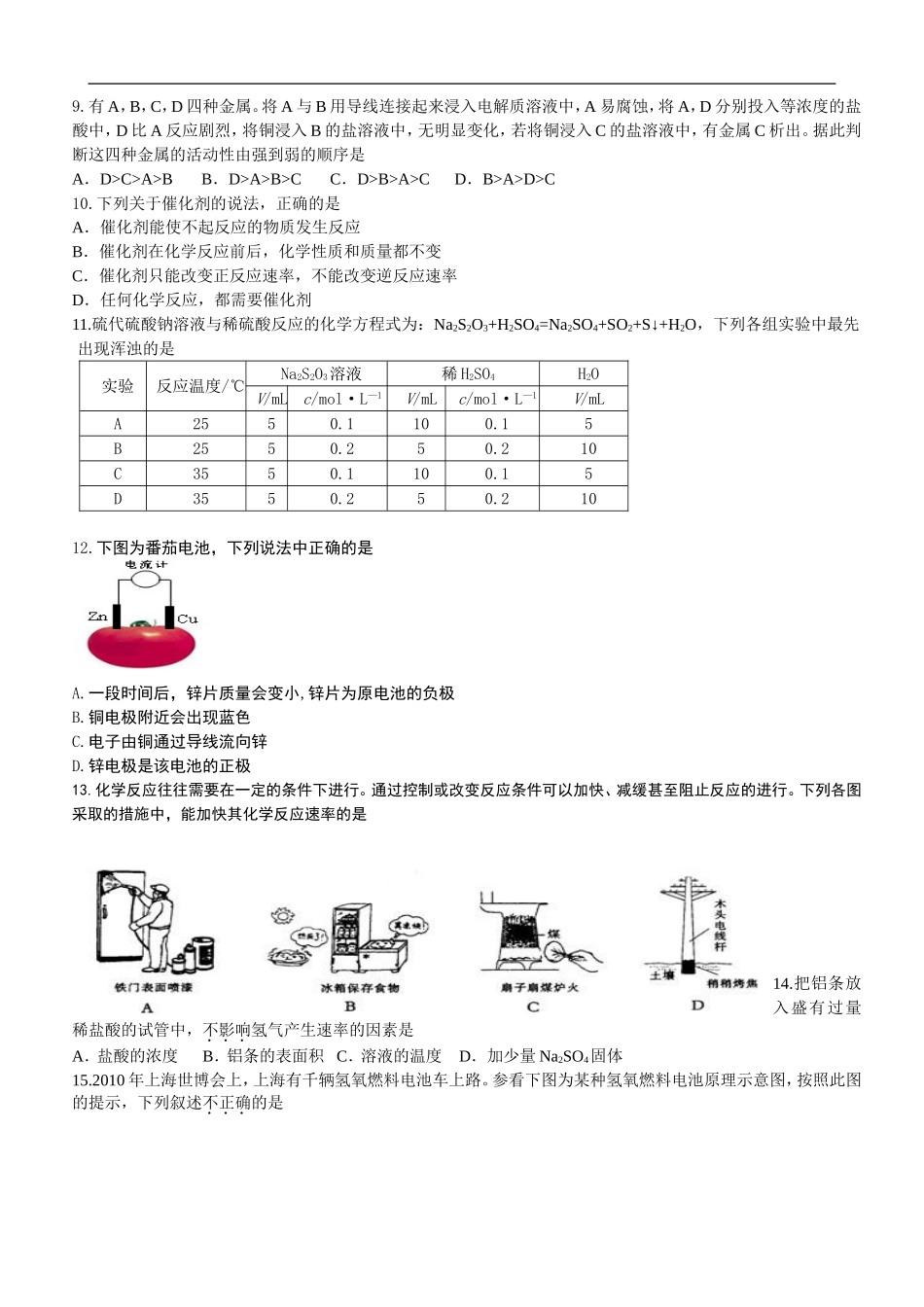
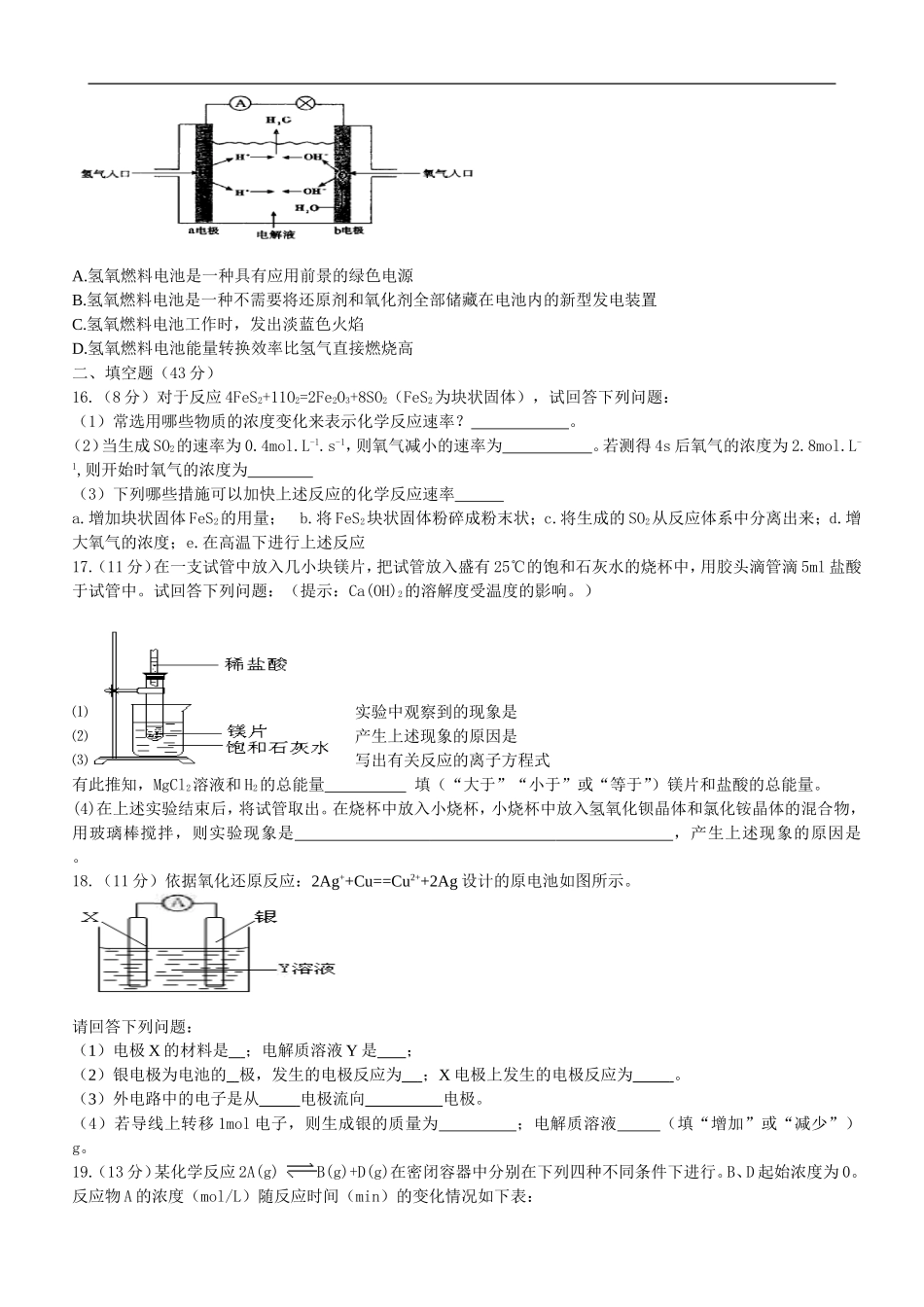
《化学反应与能量》单元测试题一、选择题(每小题3分,共15小题,共45分;每小题只有一个选项正确。)1.下列说法正确的是A.需要加热的化学反应都是吸热反应B.中和反应都是放热反应C.原电池是将电能转化为化学能的装置D.当可逆反应达到化学平衡时,正逆反应速率都为零。2.有下列物质:①NaOH固体;②浓硫酸;③NH4NO3晶体;④CaO固体。现将它们分别装入有水的锥形瓶里,立即塞紧带U形管的塞子,发现U形管内的滴有红墨水的水面呈形如右图所示状态,判断加入的物质可能是A.①②③④B.①②④C.②③④D.①②③3.下列反应既是氧化还原反应又是吸热反应的是A.铜和浓硝酸反应B.Ba(OH)2.8H2O与NH4Cl的反应C.灼热的碳与二氧化碳反应D.甲烷在氧气中的燃烧反应4.对于可逆反应N2+3H22NH3,下列各关系中不能说明该反应已达到平衡状态的是A.单位时间内,生成2molNH3同时消耗1molN2B.反应混合物中,氨气的浓度不再变化C.2v正(H2)=3v逆(NH3)D.反应混合物中,氮气的百分含量不再发生变化5.为了说明影响化学反应速率快慢的因素,甲、乙、丙、丁四位同学分别设计了如下四个实验,你认为结论不正确的是A.将大小、形状完全相同的镁条和铝条分别与相同浓度的盐酸反应时,两者的速率一样大B.在相同条件下,等质量的大理石块和大理石粉末分别与相同浓度的盐酸反应时,大理石粉末反应速率快C.将浓硝酸分别放在冷暗处和强光照射下,会发现光照可以加快浓硝酸的分解D.两只试管中分别加入相同质量的氯酸钾,其中一只试管中再加入少量二氧化锰,同时加热,产生氧气的快慢不同。6.由铜-锌-稀硫酸构成的原电池中,当导线中有1mol电子通过时,理论上的两极变化是①锌片溶解了32.5g②锌片增重了32.5g③铜片上析出1gH2④铜片上析出1molH2A.①③B.①④C.②③D.②④7.废电池处理不当不仅造成浪费,还会对环境造成严重污染,对人体健康也存在极大的危害。有同学想变废为宝,他的以下想法你认为不正确的是A.把锌皮取下洗净用于实验室制取氢气B.碳棒取下洗净用作电极C.把铜帽取下洗净回收利用D.电池内部填有氯化铵等化学物质,将废电池中的黑色糊状物作化肥用8.2010年10月1日中国在西昌卫星发射中心用长丙三号火箭成功发射了“嫦娥2号”探月卫星,“嫦娥2号”和长丙三号火箭的推进剂是液氢和液氧。下列描述不属于用液氢作推进剂的优点的是A.氢气燃烧的产物为水,对环境无污染。B.氢气的燃烧热值高。C.氢气的制取成本低,便于贮存。D.氢气的来源丰富9.有A,B,C,D四种金属。将A与B用导线连接起来浸入电解质溶液中,A易腐蚀,将A,D分别投入等浓度的盐酸中,D比A反应剧烈,将铜浸入B的盐溶液中,无明显变化,若将铜浸入C的盐溶液中,有金属C析出。据此判断这四种金属的活动性由强到弱的顺序是A.D>C>A>BB.D>A>B>CC.D>B>A>CD.B>A>D>C10.下列关于催化剂的说法,正确的是A.催化剂能使不起反应的物质发生反应B.催化剂在化学反应前后,化学性质和质量都不变C.催化剂只能改变正反应速率,不能改变逆反应速率D.任何化学反应,都需要催化剂11.硫代硫酸钠溶液与稀硫酸反应的化学方程式为:Na2S2O3+H2SO4=Na2SO4+SO2+S↓+H2O,下列各组实验中最先出现浑浊的是实验反应温度/℃Na2S2O3溶液稀H2SO4H2OV/mLc/mol·L—1V/mLc/mol·L—1V/mLA2550.1100.15B2550.250.210C3550.1100.15D3550.250.21012.下图为番茄电池,下列说法中正确的是A.一段时间后,锌片质量会变小,锌片为原电池的负极B.铜电极附近会出现蓝色C.电子由铜通过导线流向锌D.锌电极是该电池的正极13.化学反应往往需要在一定的条件下进行。通过控制或改变反应条件可以加快、减缓甚至阻止反应的进行。下列各图采取的措施中,能加快其化学反应速率的是14.把铝条放入盛有过量稀盐酸的试管中,不影响氢气产生速率的因素是A.盐酸的浓度B.铝条的表面积C.溶液的温度D.加少量Na2SO4固体15.2010年上海世博会上,上海有千辆氢氧燃料电池车上路。参看下图为某种氢氧燃料电池原理示意图,按照此图的提示,下列叙述不正确的是A.氢氧燃料电池是一种具有应用前景的绿色电源B.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置C.氢氧燃料电池工作时,...