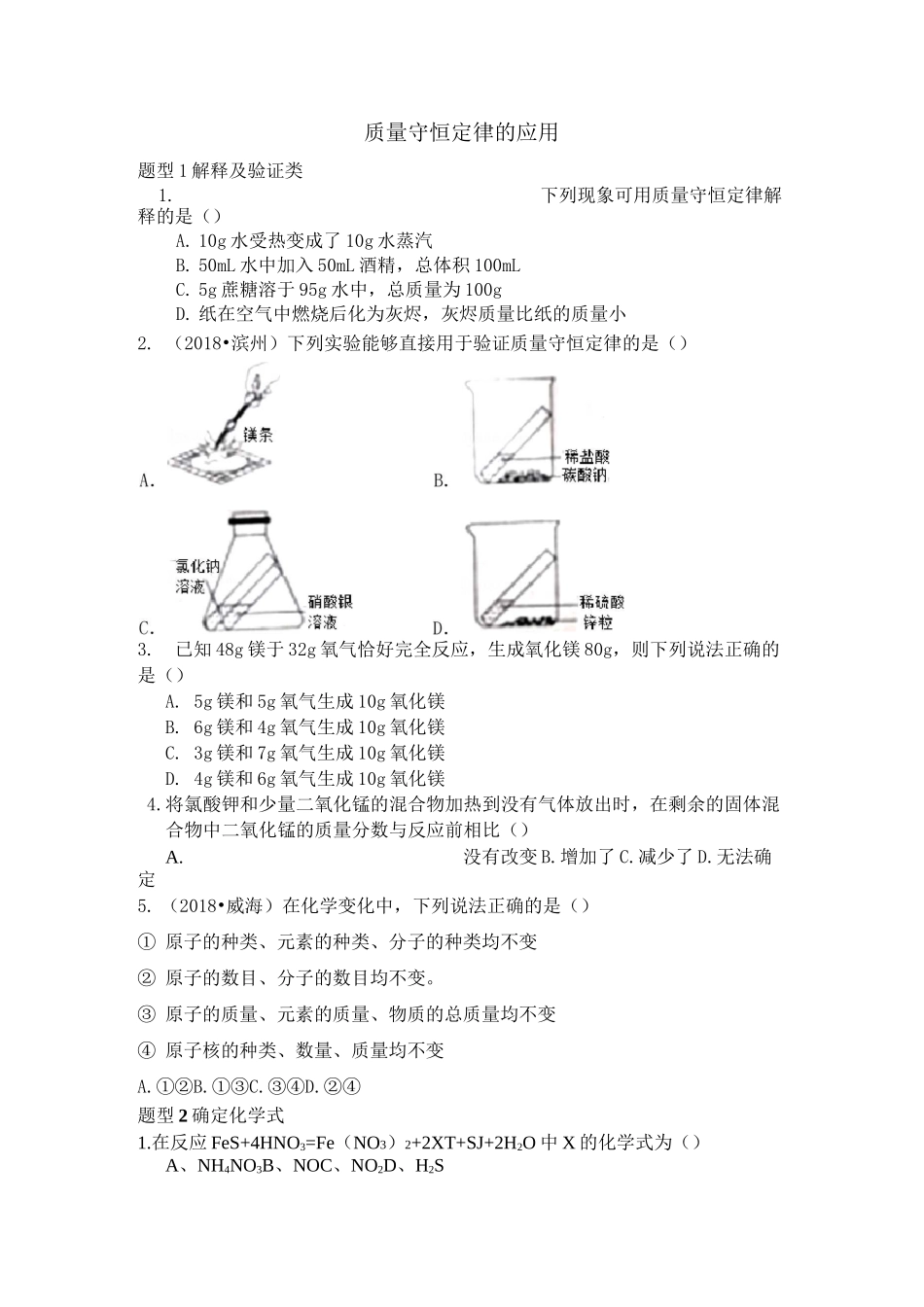
质量守恒定律的应用题型 1 解释及验证类1.下列现象可用质量守恒定律解释的是()A. 10g 水受热变成了 10g 水蒸汽B. 50mL 水中加入 50mL 酒精,总体积 100mLC. 5g 蔗糖溶于 95g 水中,总质量为 100gD. 纸在空气中燃烧后化为灰烬,灰烬质量比纸的质量小2. (2018•滨州)下列实验能够直接用于验证质量守恒定律的是()3.已知 48g 镁于 32g 氧气恰好完全反应,生成氧化镁 80g,则下列说法正确的是()A. 5g 镁和 5g 氧气生成 10g 氧化镁B. 6g 镁和 4g 氧气生成 10g 氧化镁C. 3g 镁和 7g 氧气生成 10g 氧化镁D. 4g 镁和 6g 氧气生成 10g 氧化镁4.将氯酸钾和少量二氧化锰的混合物加热到没有气体放出时,在剩余的固体混合物中二氧化锰的质量分数与反应前相比()A.没有改变 B.增加了 C.减少了 D.无法确定5. (2018•威海)在化学变化中,下列说法正确的是()① 原子的种类、元素的种类、分子的种类均不变② 原子的数目、分子的数目均不变。③ 原子的质量、元素的质量、物质的总质量均不变④ 原子核的种类、数量、质量均不变A.①②B.①③C.③④D.②④题型 2 确定化学式1.在反应 FeS+4HNO3=Fe(NO3)2+2XT+SJ+2H2O 中 X 的化学式为()A、NH4NO3B、NOC、NO2D、H2SA.X2B.X2YC.XY2D.XY33.我C.一定含有碳、氢、氧三种元素 D.只含有碳元素2.根据质量守恒定律判断,在 2XY2+Y2=2Z 的反应中,,的化学式应该是()是偏二甲肼(用 R 表示),其燃烧的化学方程式为:R+2N2O4=3N2+4H2O+2CO2,则偏二甲肼的化学式是()A.C2H8N2B.N2H4C.CH4D.C6H7N282244674.某元素 R 的氧比物中,R 元素与氧元素的质量比为 7:8,R 的相对原子质量为14,则 R 氧化物的化学式是()A.ROB.ROC.ROD.RO22255、3Cu+8HNO3==3Cu(NO3)2+2Xt+4H20,求 X 的化学式为。6、(2018•苏州)高锰酸钾和浓盐酸发生如下应:2KMnO+16HCl=2KCl+2MnCl+5X42t+8H0,根据质量守恒定律,推测 X 应是()2A.HClOB.ClOC.OD.Cl2227、4K2Cr2O8==4K2CrO4+2R+3O2求 R 的化学式为题型 3 计算相对分子质量1.有化学反应 3A+B=C+3D,已知 A、B、C 的相对分子质量分别为 98、160、400,D 的相对分子质量为。2. 在化学反应 3X+4Y=2Z 中,已知 X 和 Z 的相对分子质量分别是 32 和 102,则 Y 的相对分子质量为。题型 4 求反应物或生成物化学式前的系数1.2008 年奥运会“祥云”火炬中燃料燃烧后不会对环境造成污染,体现了...