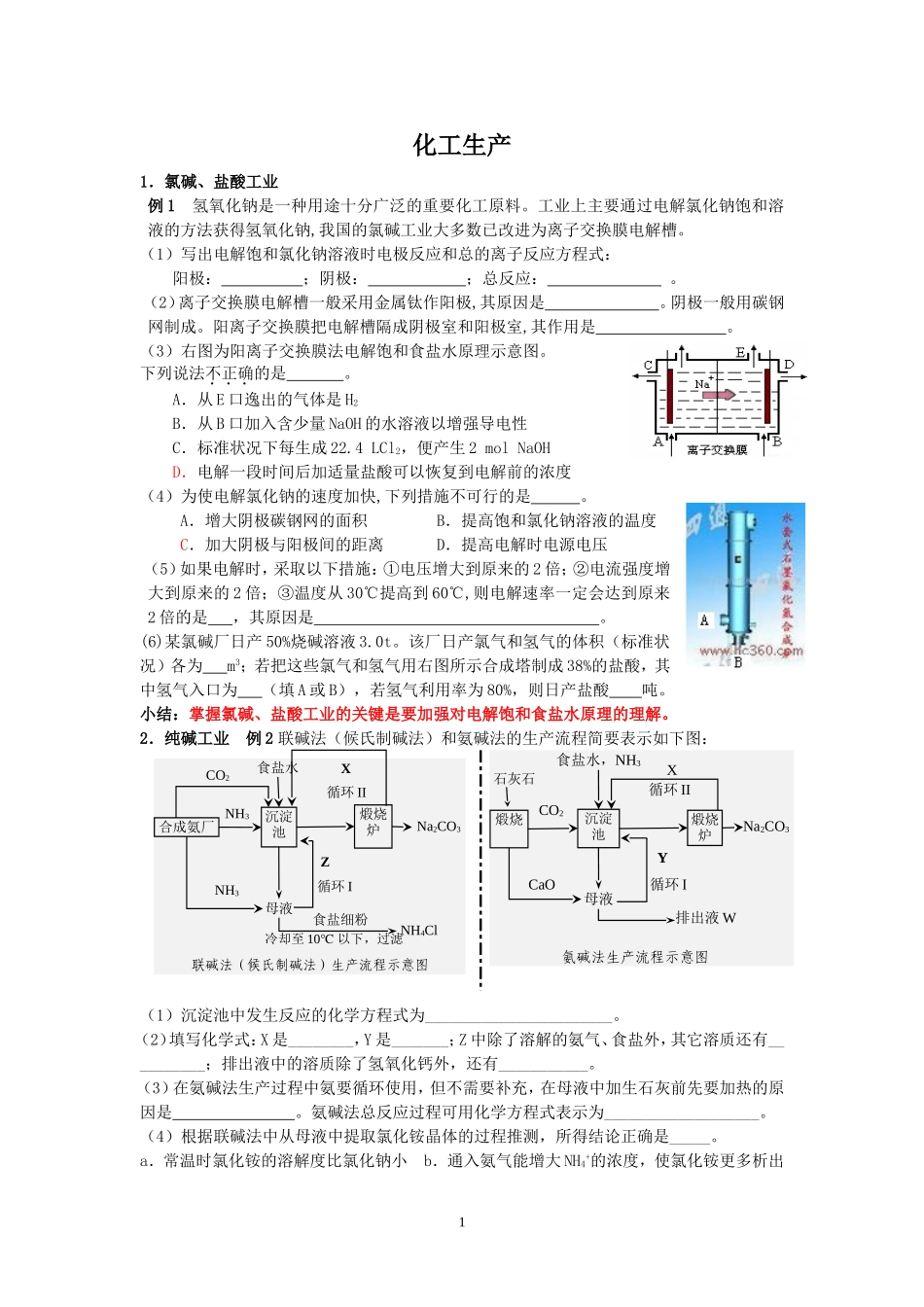
CO2Na2CO3X食盐水循环II循环I母液NH4Cl煅烧炉合成氨厂沉淀池NH3NH3食盐细粉Z冷却至10℃以下,过滤联碱法(候氏制碱法)生产流程示意图CO2Na2CO3X食盐水,NH3母液煅烧炉煅烧沉淀池CaOY排出液W循环II循环I氨碱法生产流程示意图石灰石化工生产1.氯碱、盐酸工业例1氢氧化钠是一种用途十分广泛的重要化工原料。工业上主要通过电解氯化钠饱和溶液的方法获得氢氧化钠,我国的氯碱工业大多数已改进为离子交换膜电解槽。(1)写出电解饱和氯化钠溶液时电极反应和总的离子反应方程式:阳极:;阴极:;总反应:。(2)离子交换膜电解槽一般采用金属钛作阳极,其原因是。阴极一般用碳钢网制成。阳离子交换膜把电解槽隔成阴极室和阳极室,其作用是。(3)右图为阳离子交换膜法电解饱和食盐水原理示意图。下列说法不正确的是。A.从E口逸出的气体是H2B.从B口加入含少量NaOH的水溶液以增强导电性C.标准状况下每生成22.4LCl2,便产生2molNaOHD.电解一段时间后加适量盐酸可以恢复到电解前的浓度(4)为使电解氯化钠的速度加快,下列措施不可行的是。A.增大阴极碳钢网的面积B.提高饱和氯化钠溶液的温度C.加大阴极与阳极间的距离D.提高电解时电源电压(5)如果电解时,采取以下措施:①电压增大到原来的2倍;②电流强度增大到原来的2倍;③温度从30℃提高到60℃,则电解速率一定会达到原来2倍的是,其原因是。(6)某氯碱厂日产50%烧碱溶液3.0t。该厂日产氯气和氢气的体积(标准状况)各为m3;若把这些氯气和氢气用右图所示合成塔制成38%的盐酸,其中氢气入口为(填A或B),若氢气利用率为80%,则日产盐酸吨。小结:掌握氯碱、盐酸工业的关键是要加强对电解饱和食盐水原理的理解。2.纯碱工业例2联碱法(候氏制碱法)和氨碱法的生产流程简要表示如下图:(1)沉淀池中发生反应的化学方程式为_______________________。(2)填写化学式:X是________,Y是_______;Z中除了溶解的氨气、食盐外,其它溶质还有__________;排出液中的溶质除了氢氧化钙外,还有___________。(3)在氨碱法生产过程中氨要循环使用,但不需要补充,在母液中加生石灰前先要加热的原因是。氨碱法总反应过程可用化学方程式表示为___________________。(4)根据联碱法中从母液中提取氯化铵晶体的过程推测,所得结论正确是_____。a.常温时氯化铵的溶解度比氯化钠小b.通入氨气能增大NH4+的浓度,使氯化铵更多析出1c.加入食盐细粉能提高Na+的浓度,使NaHCO3结晶析出d.通入氨气能使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度(5)联碱法中,每当通入NH344.8L(已折合成标准状况下)时可以得到纯碱100.0g,则NH3的利用率为______;相比于氨碱法,氯化钠的利用率从70%提高到90%以上,主要是设计了(填上述流程中的编号)。指出联碱法的另一项优点_________________。(6)绿色化学的重要原则之一是提高反应的原子利用率。根据“联合制碱法”总反应,列出计算原子利用率的表达式:原子利用率(%)=。小结:掌握纯碱工业的关键是要区别联碱法和氨碱法的异同,深入理解有关的实验原理。3.硫酸、硝酸、合成氨工业例3硫酸工业在国民经济中占有极其重要的地位。(1)硫酸的最大消费渠道是化肥工业,用硫酸制造的常见化肥有(任写一种)。(2)硫酸生产中,根据勒夏特列原理来确定的条件或措施有(填写序号)。A.矿石加入沸腾炉之前先粉碎B.使用V2O5作催化剂C.接触室中使用适宜的温度D.净化后的炉气中要有过量的空气E.催化氧化在常压下进行F.吸收塔中用98.3%的浓硫酸吸收SO3(3)在硫酸工业中,通过下列反应使二氧化硫转化为三氧化硫:2SO2(g)+O2(g)2SO3(g)+196.6kJ在实际工业生产中,常采用“二转二吸法”,即将第一次转化生成的SO2分离后,将未转化的SO2进行二次转化,假若两次SO2的转化率均为95%,则最终SO2的转化率为。(4)硫酸的工业制法涉及三个主要的化学反应及相应的设备(沸腾炉、接触室、吸收塔)。①三个设备分别使反应物之间或冷热气体间进行了“对流”。请简述接触室中冷热气体之间对流的意义:。②工业生产中常用氨—酸法进行尾气脱硫,以达到消除污染、废物利用的目的。用化学方程式表示其反应原理:。例4工...