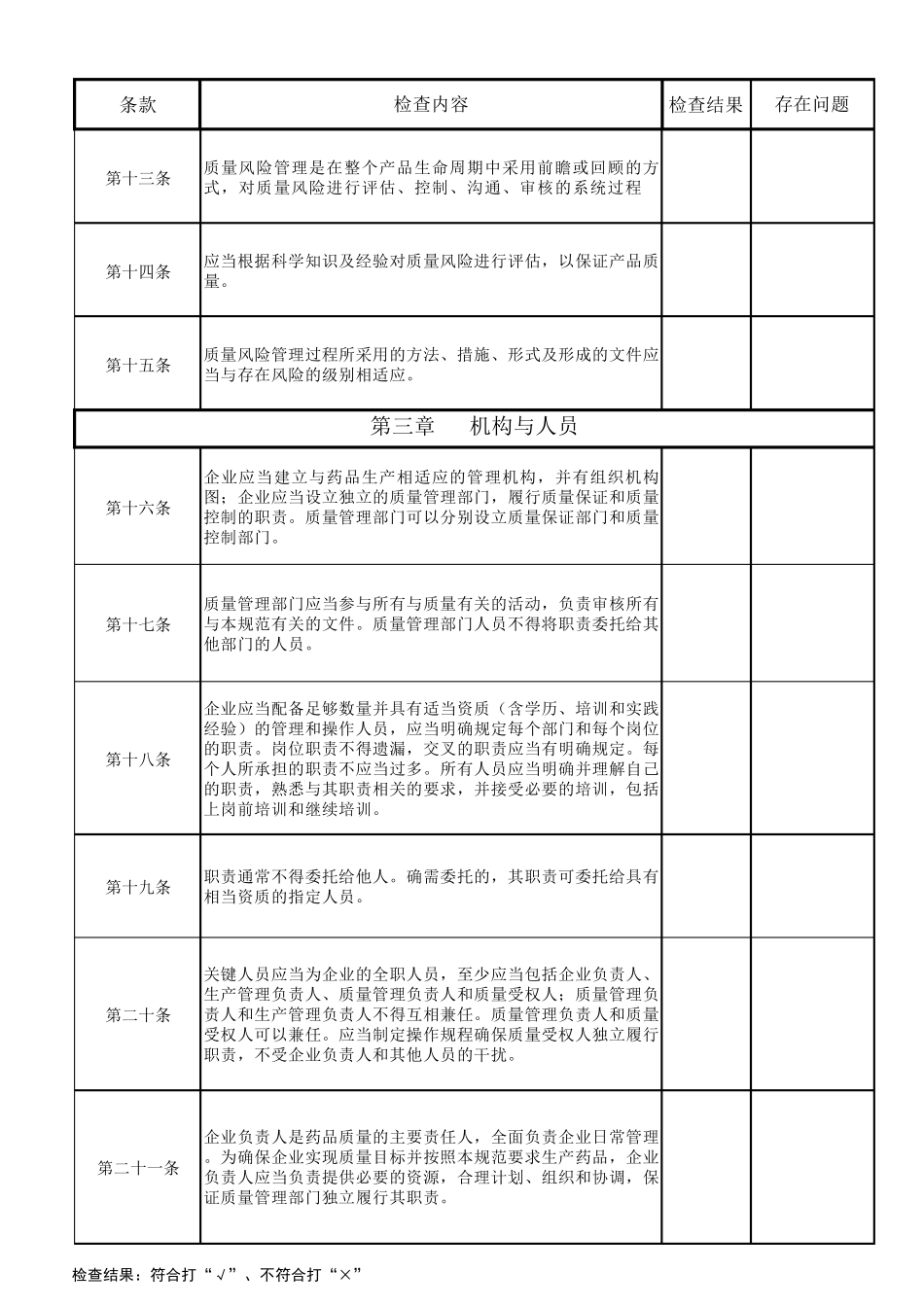
条款检查结果第二条第三条第四条第五条第六条第七条第八条第一章 总则存在问题质量保证是质量管理体系的一部分。企业必须建立质量保证系统,同时建立完整的文件体系,以保证系统有效运行企业高层管理人员应当确保实现既定的质量目标,不同层次的人员以及供应商、经销商应当共同参与并承担各自的责任。企业应当配备足够的、符合要求的人员、厂房、设施和设备,为实现质量目标提供必要的条件。第九条 (四)采购和使用的原辅料和包装材料正确无误;(九)在贮存、发运和随后的各种操作过程中有保证药品质量的适当措施;(十)按照自检操作规程,定期检查评估质量保证系统的有效性和适用性。质量保证系统应当确保: (五)中间产品得到有效控制; (六)确认、验证的实施; (七)严格按照规程进行生产、检查、检验和复核; (八)每批产品经质量受权人批准后方 可 放 行;自检检查表第二章 质量管理检查内 容企业应当建立药品质量管理体系。该 体系应当涵 盖 影 响 药品质量的所 有因 素 ,包括 确保药品质量符合预 定用途 的有组 织、有计 划 的全 部活 动 。本 规范 作为质量管理体系的一部分,是药品生产管理和质量控制的基 本 要求,旨 在最 大 限 度 地 降 低 药品生产过程中污 染、交 叉 污 染 以及混 淆 、差 错 等 风 险 ,确保持 续 稳 定地 生产出符合预 定用途 和注 册 要求的药品。企业应当严格执 行本 规范 ,坚 持 诚 实守 信 ,禁 止 任何 虚 假 、欺 骗 行为。企业应当建立符合药品质量管理要求的质量目标,将 药品注 册的有关 安 全 、有效和质量可 控的所 有要求,系统地 贯 彻 到药品生产、控制及产品放 行、贮存、发运的全 过程中,确保所 生产的药品符合预 定用途 和注 册 要求 (一)药品的设计 与研 发体现本 规范 的要求; (二)生产管理和质量控制活 动 符合本 规范 的要求; (三)管理职 责明 确;检查结果:符合打“√”、不符合打“×”1/31条款检查结果存在问题检查内容第十一条 3.适用的设备和维修保障; 4.正确的原辅料、包装材料和标签; 5.经批准的工艺规程和操作规程; 1.具有适当的资质并经培训合格的人员; 2.足够的厂房和空间; (二)生产工艺及其重大变更均经过验证;第十条 (五)操作人员经过培训,能够按照操作规程正确操作; (三)配备所需的资源,至少包括:(一)制定生产工艺...